��Ŀ����
20��֣�����Ľ���ʹ֣�ݵ���������и��ӷ��㣮��1��������Dz������Ͻ���϶����ô�����ԭ�������Ͻ��Ӳ�ȱȴ��������������Ҫ�����ĸ�������д����ҵ���ó����������Ļ�ѧ����ʽΪ3CO+Fe2O3$\frac{\underline{\;����\;}}{\;}$3CO2+2Fe��
��2��ÿ������ʴ�����ϵ�����ƷԼռ�������20%��40%�����ڿ�������ʴ��ʵ���������������е�ˮ��������ͬ���õĽ����
��3����ҵ�ϳ���ϡ��������⣬д���÷�Ӧ�Ļ�ѧ����ʽFe2O3+6HCl�T2FeCl3+3H2O��
��4������ͬѧ��ϡ�������һ����Һ����֤��Mg��Fe��Cu��Ag���ֽ����Ļ��˳�������μ����ģ���ش��������⣺
�ٿ������õ���һ����Һ����������Һ��
��˵��Cu��Ag���õ�ʵ������ͭ˿������һ������ɫ�������ɣ�
��5����ʵ�������ȡ3.25gп�����ձ��У������м���50gһ������������ϡ���ᣬǡ����ȫ��Ӧ����ϡ���������ʵ����������Ƕ��٣�
���� ��1�����ݺϽ�����ʽ��з��������ݹ�ҵ������һ����̼����������Ӧ�������Ͷ�����̼������
��2�������������������������
��3�������������������ᷴӦ�����Ȼ�����ˮ���
��4�����ݽ������˳�������Ӧ�÷�������ǰ�Ľ��������ᷴӦ����������λ����ǰ�Ľ����ܽ�λ�����Ľ�����������Һ���û�������
��5�����ݻ�ѧ����ʽ����Һ���������ļ��㷽��������
��� �⣺��1���Ͻ��������Ĵ�������Ӳ�ȴ������Ͻ���ϵ�Ӳ�ȱȴ�����������������Ͻ���϶����ô�������ҵ����һ����̼��ԭ��������������Ҫ������CO�Ļ�ԭ�ԣ��ڸ����º���������Ӧ�������Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪ3CO+Fe2O3$\frac{\underline{\;����\;}}{\;}$3CO2+2Fe��
�ʴ�Ϊ�����Ͻ��Ӳ�ȴ��ڴ�����3CO+Fe2O3$\frac{\underline{\;����\;}}{\;}$3CO2+2Fe��
��2�����ڿ�������ʴ��ʵ���������������е�ˮ��������ͬ���õĽ����
�ʴ�Ϊ��ˮ��������
��3���������������ᷴӦ�����Ȼ�����ˮ���÷�Ӧ�Ļ�ѧ����ʽΪ��Fe2O3+6HCl=2FeCl3+3H2O��
�ʴ�Ϊ��Fe2O3+6HCl=2FeCl3+3H2O��
��4�����ɽ������˳�������Ӧ�ÿ�֪������ϡ�������ȿ���֤þ�������ã�þ������ͭ�������ã���Ϊϡ�������þ�ܷ�Ӧ������������ͭ����ϡ�����Ӧ��������������þ���������������ٶȿ죮��������֤ͭ�����Ľ�����ԣ����ý����˳�����ǰ��Ľ����ܰѺ���Ľ��������Ļ��������Һ���û�������������������Һ���Ƚ�ͭ���Ļ�ԣ�
��˵��Cu��Ag���õ�ʵ�������ǣ�ͭ˿������������Һ�У�ͭ˿�ı��������Ľ������ɣ�
�������������Һ ��ͭ˿������һ������ɫ�������ɣ�
��5���裺ϡ���������ʵ���������ΪX
Zn+H2SO4=ZnSO4+H2��
65 98
3.25g 50g��X
$\frac{65}{98}=\frac{3.25g}{50g•X}$
X=9.8%
��ϡ���������ʵ���������Ϊ9.8%��
���� ���⿼�������Ͻ�����ʣ���ѧ����ʽ����д�������Ļ�ԣ����ݻ�ѧ����ʽ�ļ���ȣ�Ҫ�������գ�

 ״Ԫ��ȫ��ͻ�Ƶ�����ϵ�д�
״Ԫ��ȫ��ͻ�Ƶ�����ϵ�д� ֱͨ������У�ܲ��¿�ֱͨ��Уϵ�д�
ֱͨ������У�ܲ��¿�ֱͨ��Уϵ�д� �ƽ�����ϡ�С�����غ���˿��صĽ���֮һ�������������ɵ����������������Ķ�����ͼ��ʾ���ǽ���Ԫ�����ڱ��еIJ�����Ϣ�������ͼʾ���ݲ������ѧ֪ʶ�жϣ����й��ڽ��˵���У�����ȷ���ǣ�������
�ƽ�����ϡ�С�����غ���˿��صĽ���֮һ�������������ɵ����������������Ķ�����ͼ��ʾ���ǽ���Ԫ�����ڱ��еIJ�����Ϣ�������ͼʾ���ݲ������ѧ֪ʶ�жϣ����й��ڽ��˵���У�����ȷ���ǣ�������| A�� | ������Ȼ���п����Ե�����ʽ���� | B�� | ������ԭ������Ϊ197.0 | ||
| C�� | ������ԭ������Ϊ79 | D�� | ���ԭ������Ϊ79 |
| A�� | ��ˮ�������ʯ�ҡ����� | B�� | ʯ�͡�ú����Ȼ�� | ||
| C�� | �ྻ�Ŀ������Ȼ��ơ����� | D�� | ����ƾ���������ʯ |
| A�� | ��̼������ĭ����̼Ԫ����� | B�� | ��̼������ĭ���ܱ��������� | ||
| C�� | ��̼������ĭ���ͽ��ʯ��������ͬ | D�� | ��̼������ĭ���ܸ���ˮ���� |
| A�� | ��Һ������ɫ������ | |
| B�� | ��һ���ȶ���Һ�嶼����Һ | |
| C�� | �����Է��ӻ����ӵ���ʽ��ɢ���ܼ��� | |
| D�� | ˮ�����ܽ��κ����� |
 �÷��ű�ʾ��
�÷��ű�ʾ��

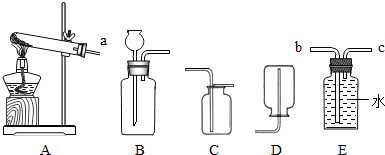 Ϊ����ȡ�����Ͷ�����̼��ʵ�����ṩ������ҩƷ������װ�ã�
Ϊ����ȡ�����Ͷ�����̼��ʵ�����ṩ������ҩƷ������װ�ã�