题目内容
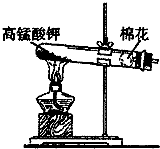
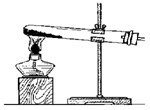
把10克的氯酸钾与二氧化锰混合物再试管中加热,待完全反应后冷却,称得剩余固体为6.16克.求:
(1)根据质量守恒定律可得氧气多少克?
(2)剩余固体中含那些物质,各多少克?
(1)根据质量守恒定律可得氧气多少克?
(2)剩余固体中含那些物质,各多少克?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:据质量守恒定律,计算出反应生成氧气的质量,利用氯酸钾分解的化学方程式和氧气的质量,列出比例式,就可计算出分解的氯酸钾的质量,进而求出原混合物中氯酸钾的质量,然后用混合物质量减去混合物中氯酸钾的质量就是二氧化锰的质量(二氧化锰是催化剂,不参与反应,反应前后质量不变.
解答:解:(1)依据质量守恒定律可知:生成O2 的质量=10g-6.16g=3.84g
(2)设生成的氯化钾质量为x
2KClO3
2KCl+3O2↑
149 96
x 3.84g
=
x=5.96g
则剩余的固体中二氧化锰的质量=6.16g-5.96g=0.2g
答:(1)据质量守恒定律可得氧气为3.84g;(2)剩余固体中氯化钾和二氧化锰的质量分别为5.96g和0.2g.
(2)设生成的氯化钾质量为x
2KClO3
| ||
| △ |
149 96
x 3.84g
| 149 |
| x |
| 96 |
| 3.84g |
x=5.96g
则剩余的固体中二氧化锰的质量=6.16g-5.96g=0.2g
答:(1)据质量守恒定律可得氧气为3.84g;(2)剩余固体中氯化钾和二氧化锰的质量分别为5.96g和0.2g.
点评:本题主要考查学生利用化学方程式进行计算的能力.要正确解答本题,关键是要知道二氧化锰是催化剂,不参与反应,反应前后质量不变.

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
我国新修订的《环境空气质量标准》增加了PM2.5监测指标,PM2.5是指大气中直径小于或等于2.5微米的可吸入颗粒物,它是造成雾霾天气的“元凶”之一.下列做法不会改变PM2.5检测结果的是( )
| A、使用太阳能热水器 |
| B、燃放鞭炮 |
| C、露天焚烧垃圾、秸秆 |
| D、工厂排放烟尘 |
下列有关空气各成分的说法正确的是( )
| A、氧气的化学性质比较活泼,属于可燃物 |
| B、氮气的化学性质不活泼,可用于食品防腐 |
| C、洁净的空气是纯净物 |
| D、空气中的稀有气体没有任何价值 |
下列试剂瓶标签写错误的是( )
A、 |
B、 |
C、 |
D、 |