题目内容
6.草酸晶体(H2C2O4•xH2O)在常温下是一种无色透明晶体.草酸晶体受热时分解的化学方程式为:H2C2O4•xH2O$\frac{\underline{\;\;△\;\;}}{\;}$(x+1)H2O+CO2↑+CO↑某化学兴趣小组的同学利用该信息以及所学的知识设计并开展实验,测定草酸晶体分子中X的值.(图中固定装置已略去,装置气密性良好,装置A、B中的试剂足量,注射器量程足够)
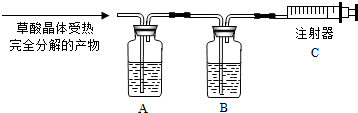
Ⅰ.测量装置A、B的质量,排尽注射器中的空气,连接装置;
Ⅱ.取质量为m的草酸晶体,加热至完全分解,将产物全部通入以上装置;
Ⅲ.测量并记录装置A增加的质量为a,装置B增加的质量为b,装置C读数为V;
Ⅳ.甲乙两位同学想利用上述所得数据计算求X.
请回答下列问题:
(1)装置A中盛放的液体是浓硫酸;装置C的作用之一是测量CO的体积.
(2)甲同学依据装置A测量结果,列出计算草酸晶体分子(H2C2O4•xH2O)中X为$\frac{5a-m}{m-a}$(用含题中相关字母的代数式表示).
(3)乙同学对甲同学的计算结果的可靠性进行反思与评价,认为反应后装置A中残留的气体会使计算结果偏大(填“偏小”或“偏大”).
分析 (1)根据加热后的产物来分析,A是用来吸收生成的水蒸气、B是吸收生成的二氧化碳,C是收集生成的一氧化碳;
(2)根据参加反应的草酸晶体以及生成水的质量,利用化学方程式进行计算;
(3)根据题意,A中残留气体中含有少量的二氧化碳;
解答 解:
(1)装置A中盛放的液体是吸收生成的水蒸气,应该用浓硫酸;吸收生成的二氧化碳气体用浓氢氧化钠溶液;最后剩余的一氧化碳气体进入注射器;
(2)H2C2O4•xH2O$\frac{\underline{\;\;△\;\;}}{\;}$(x+1)H2O+CO2↑+CO↑
90+18x 18(x+1)
m a
$\frac{(90+18m)}{18(x+1)}=\frac{m}{a}$
x=$\frac{5a-m}{m-a}$
(3)气体部分残留在A中,导致少量的二氧化碳没有被B装置完全吸收,A质量偏大,导致测量结果偏大,故填:偏大;
答案:(1)浓硫酸;CO; (2)$\frac{5a-m}{m-a}$;(3)偏大.
点评 本题属于信息题的考查,解题的关键是依据题目的信息结合相关的知识进行分析,本题要求熟练运用二氧化碳、一氧化碳、水等的性质并能根据化学方程式进行分析和计算.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
16.化学概念的正确理解,是学好化学的关键,下列说法错误的是( )
| A. | 一种元素与一种元素的根本区别是质子数不同 | |
| B. | 电解水的实验说明在化学反应中,分子改变了,但原子种类和数目没变 | |
| C. | O2,CO2,SO2中都含有O元素 | |
| D. | 相对原子质量就是原子的质量 |
17.化学用语是我们学习和研究化学的重要语言工具.请用化学用语填写如表.
| 甲烷 | n个铁原子 | 氢氧根离子 | 正二价的锌元素 |
| CH4 | nFe | OH- | $\stackrel{+2}{Zn}$ |
18.在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如表:下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量/g | 54 | 17 | 20 | 10 |
| 反应后的质量/g | 10 | 0 | 2 | x |
| A. | x为89 | B. | 参加反应的丙物质的质量为20 g | ||
| C. | 该反应为分解反应 | D. | 甲物质全部反应完 |
15.硫酸亚铁铵晶体俗名为摩尔盐,在制药、电镀方面有广泛的应用.
资料:①硫酸亚铁铵晶体化学式为FeSO4•(NH4)2SO4•6H2O,相对分子质量为392,易溶于水,不溶于乙醇;
②相关物质的溶解度(单位:g)如表:
③硫酸亚铁铵晶体受热时,在200℃以下只有结晶水失去.
某兴趣小组的学生用含有少量铜的废铁屑制备硫酸亚铁铵晶体,流程如图:
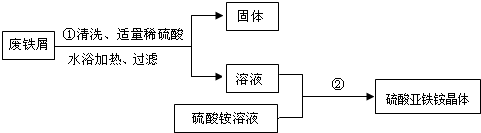
(1)操作①中发生反应的化学方程式为Fe+H2SO4═FeSO4+H2↑;
(2)过滤所需的玻璃仪器有烧杯、玻璃棒、漏斗;
(3)操作①中过滤时,要趁热进行的原因是防止温度降低FeSO4晶体析出,产量(产率)降低或使FeSO4尽可能多的溶解,提高产量(产率);
(4)操作②的目的是得到硫酸亚铁铵晶体.操作顺序是b→c→a→d;
a.过滤 b.加热浓缩 c.冷却结晶 d.洗涤干燥
(5)操作②中使用乙醇洗涤,可快速晾干.这样做的优点是AB;
A.避免用水洗涤所造成的晶体损耗
B.酒精易挥发,可低温晾干晶体
(6)该实验取废铁屑15g,最终得到硫酸亚铁铵晶体39.2g,则原废铁屑中铁元素的质量分数不低于37.3(精确到0.1%,不要求写过程).
资料:①硫酸亚铁铵晶体化学式为FeSO4•(NH4)2SO4•6H2O,相对分子质量为392,易溶于水,不溶于乙醇;
②相关物质的溶解度(单位:g)如表:
| 温度/℃ | FeSO4 | (NH4)2SO4 | FeSO4•(NH4)2SO4•6H2O |
| 10 | 20.0 | 73 | 17.2 |
| 20 | 26.5 | 75.4 | 21.6 |
| 30 | 32.9 | 78 | 28.1 |
某兴趣小组的学生用含有少量铜的废铁屑制备硫酸亚铁铵晶体,流程如图:

(1)操作①中发生反应的化学方程式为Fe+H2SO4═FeSO4+H2↑;
(2)过滤所需的玻璃仪器有烧杯、玻璃棒、漏斗;
(3)操作①中过滤时,要趁热进行的原因是防止温度降低FeSO4晶体析出,产量(产率)降低或使FeSO4尽可能多的溶解,提高产量(产率);
(4)操作②的目的是得到硫酸亚铁铵晶体.操作顺序是b→c→a→d;
a.过滤 b.加热浓缩 c.冷却结晶 d.洗涤干燥
(5)操作②中使用乙醇洗涤,可快速晾干.这样做的优点是AB;
A.避免用水洗涤所造成的晶体损耗
B.酒精易挥发,可低温晾干晶体
(6)该实验取废铁屑15g,最终得到硫酸亚铁铵晶体39.2g,则原废铁屑中铁元素的质量分数不低于37.3(精确到0.1%,不要求写过程).
5.今年4月22日是第47个世界地球日,今年的活动主题为“节约集约利用资源,倡导绿色简约生活”.下列做法不符合这一主题的是( )
| A. | 盗版光盘改焚烧处理为粉碎回收,二次利用 | |
| B. | 生活中一水多用,用淘米水浇花 | |
| C. | 大力发展公共交通,减少机动车尾气排放 | |
| D. | 工业污水灌入地下,减少地表水污染 |