题目内容
在天平的两个托盘上分别放两个盛有相同浓度、相同体积的稀硫酸的烧杯,调节天平平衡,然后向两烧杯中分别加入相同质量(wg)的锌和铁,原来平衡的天平有何变化?为什么?分析:本题可利用烧杯中反应前后的质量差来判断天平是否平衡,则需要根据金属与酸反应的化学方程式来计算生成的气体的质量,然后用反应前的质量和-气体的质量═反应后烧杯中的质量,若二者相等,则平衡.
解答:解:因相同浓度、相同体积的稀硫酸,则质量相等,相同质量(wg)的锌和铁,则反应可能存在三种情况:
(1)若酸不足,金属足量,则由M+H2SO4═MSO4+H2↑,酸完全反应,产生等量的气体,则由酸的质量+金属质量-气体的质量═反应后烧杯中的质量,两个反应的质量差相等,天平平衡.
(2)若酸足量,金属均不足,则设锌与酸反应生成的气体为X克,铁与酸反应生成的气体为Y克,
Zn+H2SO4═ZnSO4+H2↑,Fe+H2SO4═FeSO4+H2↑,
65 2 56 2
wg X wg Y
=
,
=
解得X═
,Y═
,
显然铁与酸产生的气体多,由酸的质量+金属质量-气体的质量═反应后烧杯中的质量,
与铁反应的烧杯一端质量小,天平不平衡,有金属锌的烧杯一端下沉.
(3)锌完全反应而铁剩余时,由于酸中的氢元素,对应锌的是完全转化为氢气,而铁对应的酸中的氢元素只是部分转化为氢气跑掉,所以导致铁一侧沉,向铁一侧倾斜.
故答案为:
(1)若酸足量,金属均不足,天平平衡;
(2)若酸足量,金属均不足,有金属锌的烧杯一端下沉;
(3)锌完全反应而铁剩余时,向铁一侧倾斜
(1)若酸不足,金属足量,则由M+H2SO4═MSO4+H2↑,酸完全反应,产生等量的气体,则由酸的质量+金属质量-气体的质量═反应后烧杯中的质量,两个反应的质量差相等,天平平衡.
(2)若酸足量,金属均不足,则设锌与酸反应生成的气体为X克,铁与酸反应生成的气体为Y克,
Zn+H2SO4═ZnSO4+H2↑,Fe+H2SO4═FeSO4+H2↑,
65 2 56 2
wg X wg Y
| 65 |
| 2 |
| wg |
| X |
| 56 |
| 2 |
| wg |
| Y |
解得X═
| 2wg |
| 65 |
| 2wg |
| 56 |
显然铁与酸产生的气体多,由酸的质量+金属质量-气体的质量═反应后烧杯中的质量,
与铁反应的烧杯一端质量小,天平不平衡,有金属锌的烧杯一端下沉.
(3)锌完全反应而铁剩余时,由于酸中的氢元素,对应锌的是完全转化为氢气,而铁对应的酸中的氢元素只是部分转化为氢气跑掉,所以导致铁一侧沉,向铁一侧倾斜.
故答案为:
(1)若酸足量,金属均不足,天平平衡;
(2)若酸足量,金属均不足,有金属锌的烧杯一端下沉;
(3)锌完全反应而铁剩余时,向铁一侧倾斜
点评:本题很难,学生对于该问题的分析可能不全面,应注意在习题中条件不是很明确的前提下,要分情况来讨论.

练习册系列答案
相关题目
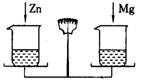
在托盘天平的两个托盘上各放一只烧杯,分别注入相同质量分数、相同质量的稀盐酸,天平平衡。向左边的烧杯中加入1 0 g金属锌,向右边的烧杯中加入1 0 g金属镁。当反应停止后,金属都有剩余,天平指针的指向是


| A.分度盘的左边 |
| B.分度盘的中间 |
| C.分度盘的右边 |
| D.3种情况都有可能 |
在托盘天平的两个托盘上各放一只烧杯,分别注入相同质量分数、相同质量的稀盐酸,天平平衡。向左边的烧杯中加入1 0 g金属锌,向右边的烧杯中加入1 0 g金属镁。当反应停止后,金属都有剩余,天平指针的指向是
| A.分度盘的左边 |
| B.分度盘的中间 |
| C.分度盘的右边 |
| D.3种情况都有可能 |