题目内容
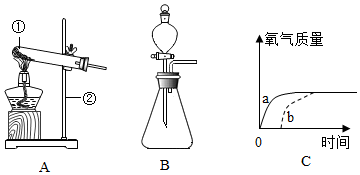
2.小华同学配制50g溶质质量分数为20%的NaCl溶液,操作流程如图1所示:
(1)小华同学应称取氯化钠的质量是10.0g.用50mL量筒量取水,实验室现有①托盘天平 ②量筒 ③烧杯 ④玻璃棒 ⑤酒精灯等仪器.(3)配制溶液过程中,上述仪器不需要的是⑤(填序号).
(2)在用托盘天平称取食盐的过程中,发现指针已偏向分度盘左侧,他接下来的操作是在左盘上减少氯化钠,直至天平平衡.
(3)在用量筒量取水的过程中,当液面接近刻度线时,他的操作如图2所示,其中规范的是C(填序号).
(4)该同学将配制的溶液装入试剂瓶中,请你帮助他在如图3所示的标签内填写好标签的内容.
(5)如果小华配制的氯化钠溶液的溶质质量分数小于20%,则造成此误差的可能原因有AB(填序号).
A.称量前天平没有调平
B.称量纸上残留少量NaCl
C.向烧杯中加水时,有少量水溅出烧杯外.
分析 (1)根据溶液质量和溶质质量分数计算溶质质量;
(2)考虑天平的使用方法;天平向左偏,说明药品取的多;
(3)量取液体读数时,视线要与凹液面最低处相平;
(4)运用标签内容包括:溶液名称和溶质质量分数分析;
(5)配制溶液的质量分数小于所要配制的20%,可判断所配制的溶液中溶质氯化钠质量偏小或溶剂水的量偏大导致的结果,因此,在分析造成误差的原因时,应围绕这样两个原因分析可能造成误差的操作.
解答 解:(1)溶质质量=溶液质量×溶质质量分数=50g×20%=10.0g,水的质量为50g-10g=40g,所以需要水的体积为40mL,用50mL量筒量取水,实验室现有①托盘天平、②量筒、③烧杯、④玻璃棒、⑤酒精灯等仪器.配制溶液过程中,上述仪器不需要的是酒精灯;
(2)天平向左偏,说明氯化钠取的多,要在左盘上减少氯化钠,直至天平平衡;
(3)量取液体读数时,视线要与凹液面最低处相平,A读数方法不对,C中视线不到40mL,故选C;
(4)标签内容包括:溶液名称和溶质质量分数,故答案为 ;
;
(5)配制溶液的质量分数偏小,可能是氯化钠称量的少或加入的水多,故选AB.
故答案为:
(1)10.0g;50;
(2)在左盘上减少氯化钠,直至天平平衡;
(3)C;
(4) ;
;
(5)AB.
点评 熟练掌握配制溶液的步骤,仪器,溶质的质量分数计算是解答此题的基础和关键.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
12.物质不属于氧化物的是( )
| A. | K2MnO4 | B. | MnO2 | C. | H2O | D. | CO2 |
7.如图是元素周期表中铝元素的部分信息,和铝原子结构示意图.则下列说法不正确的是( )


| A. | 铝元素原子核内质子数为13. | |
| B. | 铝的相对原子质量为26.98 | |
| C. | 化学反应中铝原子易失电子变为 Al3+ | |
| D. | 元素在化合物中的化合价为+3价或+5价 |
11.金属钛(Ti)抗腐蚀性能好,露置于空气中数年,仍光亮如初.以金红石(主要成分是TiO2)为原料生产金属钛的步骤主要有:①在高温下,向金红石与焦炭的混合物中通入氯气(Cl2),得到TiCl4和一种可燃性气体;②在稀有气体环境和加热条件下,用Mg 与TiCl4反应得到Ti 和MgCl2.下列说法不正确…的是高温( )
| A. | ①中的反应为TiO2+C+2Cl2═TiCl4+CO2 | |
| B. | ②中稀有气体的作用是隔绝空气 | |
| C. | ①②中发生的反应都不是化合反应 | |
| D. | 金属钛在常温下不与O2反应 |