题目内容
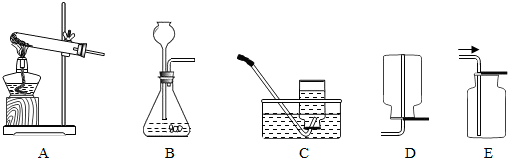
16.下列为实验室常用的实验装置,回答问题:
(1)用锌和稀硫酸制取氢气,应选用的发生装置是B(填序号,下同),收集装置是C或E.
(2)实验室常用稀盐酸和石灰石反应制CO2,该反应的化学方程式CaCO3+2HCl=CaCl2+CO2↑+H2O;
此外,也可用加热碳酸氢钠(NaHCO3)固体(产物为碳酸钠、二氧化碳、水)来制取CO2,该反应的化学方程式Na2CO3+2HCl=2NaCl+CO2↑+H2O,若用此法来制取CO2,应选用的发生装置为B,收集装置为D.
(3)如图2所示装置可用来测量生成的CO2的体积,其中在水面上放一层植物油的目的是防止CO2溶于水,植物油上方原有的空气对实验结果无(填“有”或“无”)明显影响.
分析 (1)用锌和稀硫酸制取氢气的发生装置,符合制取二氧化碳的装置:固体+液体反应,不需要加热,所以选B装置;根据氢气的性质,进行选择收集装置;
(2)实验室常用稀盐酸和石灰石来制取二氧化碳,符合制取氧气的装置:固体+固体反应,不需要加热;用加热碳酸氢钠(NaHCO3)固体来制取二氧化碳,符合制取氧气的装置:固体+固体反应,需要加热;根据二氧化碳的性质,进行选择收集装置;
(3)气体的收集:①密度小于空气,用向下排气法,如氢气;密度大于空气,用向上排气法,如二氧化碳;②氢气难溶于水,可用排水法;二氧化碳可溶于水,不能用排水法.
解答 解:(1)用锌和稀硫酸制取氢气的发生装置,固体+液体反应,不需要加热,故应选用的发生装置是B;密度小于空气,用向下排气法;氢气难溶于水,可用排水法;
(2)根据题中信息,实验室常用稀盐酸和石灰石反应制CO2,已知反应物和生成物,制取书写化学方程式,故其化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O;用加热碳酸氢钠(NaHCO3)固体来制取二氧化碳,其化学方程式为:Na2CO3+2HCl=2NaCl+CO2↑+H2O;制取二氧化碳,不需要加热,故应选用的发生装置为 B;二氧化碳密度大于空气,用向上排气法,若用此法来制取CO2,收集装置为D;
(3)如图2所示装置可用来测量生成的CO2的体积,其中在水面上放一层植物油的目的是防止CO2溶于水,植物油上方原有的空气对实验结果无明显影响.
二氧化碳可溶于水,在水面上放一层植物油的目的是.
故答为:
(1)B,C或E;
(2)CaCO3+2HCl=CaCl2+CO2↑+H2O;Na2CO3+2HCl=2NaCl+CO2↑+H2O; B,D
(4)防止CO2溶于水(造成测量不准确),(意思相近均给分),无.
点评 此题重在考察同学们对常用化学仪器的了解和识记情况,只有很好的认识它们,做试验才能得心应手;属于扩展性问题,重在考察根据物质的物理和化学性质制备物质;熟记二氧化碳的实验室制取、反应原理和其化学性质是解题的关键.

试剂:过氧化氢、二氧化锰、大理石、稀盐酸
(1)在图中的气体发生装置中,有一处错误,请改正错误长颈漏斗下端应伸入液面以下.
(2)完成下列表格:
| 制取气体 | 发生装置(填序号) | 收集装置(填序号) |
| 氧气 | ||
| 二氧化碳 |
(4)验满二氧化碳的方法是将气体通入澄清的石灰水,若澄清的石灰水变浑浊,则证明是二氧化碳.
| A. | 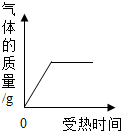 用一定质量的高锰酸钾加热制氧气 用一定质量的高锰酸钾加热制氧气 | |
| B. | 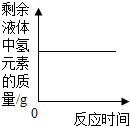 过氧化氢溶液与二氧化锰混合物制取氧气 过氧化氢溶液与二氧化锰混合物制取氧气 | |
| C. | 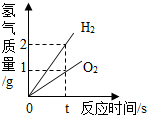 电解水实验 电解水实验 | |
| D. | 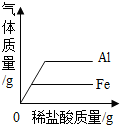 分别向等质量的铝和铁中加入溶质质量分数相同的稀盐酸至过量 分别向等质量的铝和铁中加入溶质质量分数相同的稀盐酸至过量 |
| A. |  药品称量 | B. | 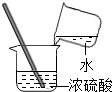 稀释浓硫酸 | C. | 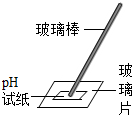 PH试纸使用 | D. | 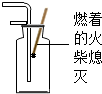 验满CO2 |
| A. | MnO2可以加快H2O2分解产生O2的速率,所以催化剂一定加快化学反应速率 | |
| B. | 钙原子核钙离子的质子数都是2O,所以质子数相同的微粒一定是同种元素 | |
| C. | 化学变化中分子一定发生改变,所以分子发生改变的变化一定是化学变化 | |
| D. | Na+、Mg2+、Cl-的最外层电子数均为8,由此得出离子的最外层电子数均为8 |
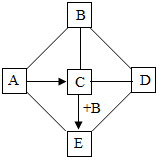 已知A-E是初中化学的常见物质.A和D是两种常见的碱;B是一种常见的酸,且只含
已知A-E是初中化学的常见物质.A和D是两种常见的碱;B是一种常见的酸,且只含