题目内容
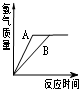 将等质量的镁粉和锌粉分别放入质量分数均为15%的稀硫酸中,产生氢气的质量随反应时间的变化曲线如图所示.下列说法正确的是
将等质量的镁粉和锌粉分别放入质量分数均为15%的稀硫酸中,产生氢气的质量随反应时间的变化曲线如图所示.下列说法正确的是
- A.A、B分别代表锌粉、镁粉
- B.反应后镁粉和锌粉一定都有剩余
- C.消耗镁粉的质量一定小于锌粉的质量
- D.消耗稀硫酸的质量不一定相等
C
分析:根据图象可以得出:①比较氢气的多少,从而可以判断出金属的相对原子质量的大小,得到氢气多的则相对原子质量小;②判断金属的活动性强弱,反应时间短或斜线斜率大的则该金属的活动性强.
解答:A、金属的活动性越强的,和酸溶液反应时产生气体的速率也就越快,根据图象不难看出,金属A完全反应后所需要的时间短,即A的活动性强,故A错误;
B、如图最终生成的氢气质量相等,则消耗的稀硫酸质量相等,而该反应中生成氢气质量相等,则Mg需要的质量多、Zn需要的质量少,已知“等质量的镁粉和锌粉”,镁可能正好反应,而锌可能剩余,故B错误;
C、对于化合价相同的金属,与酸反应时原子量越小的生成的氢气越多,所以当生成氢气一样多时,等质量的不同金属得到的氢气一样多,说明参与反应的原子量小的金属质量小原子量大的用量多,故C正确;
D、消耗稀硫酸的质量不一定相等,说法错误,因为生成的氢气相等,则消耗稀硫酸的质量一定相等,故D错误.
故选C.
点评:本题难度较大,主要考查了金属的化学性质、金属活动性顺序的应用及有关的计算,培养学生分析问题、解决问题的能力.
分析:根据图象可以得出:①比较氢气的多少,从而可以判断出金属的相对原子质量的大小,得到氢气多的则相对原子质量小;②判断金属的活动性强弱,反应时间短或斜线斜率大的则该金属的活动性强.
解答:A、金属的活动性越强的,和酸溶液反应时产生气体的速率也就越快,根据图象不难看出,金属A完全反应后所需要的时间短,即A的活动性强,故A错误;
B、如图最终生成的氢气质量相等,则消耗的稀硫酸质量相等,而该反应中生成氢气质量相等,则Mg需要的质量多、Zn需要的质量少,已知“等质量的镁粉和锌粉”,镁可能正好反应,而锌可能剩余,故B错误;
C、对于化合价相同的金属,与酸反应时原子量越小的生成的氢气越多,所以当生成氢气一样多时,等质量的不同金属得到的氢气一样多,说明参与反应的原子量小的金属质量小原子量大的用量多,故C正确;
D、消耗稀硫酸的质量不一定相等,说法错误,因为生成的氢气相等,则消耗稀硫酸的质量一定相等,故D错误.
故选C.
点评:本题难度较大,主要考查了金属的化学性质、金属活动性顺序的应用及有关的计算,培养学生分析问题、解决问题的能力.

练习册系列答案
相关题目
 将等质量的镁粉和锌粉分别放入质量分数均为15%的稀硫酸中,产生氢气的质量随反应时间的变化曲线如图所示.下列说法正确的是( )
将等质量的镁粉和锌粉分别放入质量分数均为15%的稀硫酸中,产生氢气的质量随反应时间的变化曲线如图所示.下列说法正确的是( )