题目内容
下列实验操作正确的是:
A.  测量酸碱度 B.
测量酸碱度 B. 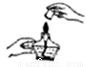 熄灭酒精灯 C.
熄灭酒精灯 C.  振荡试管 D.
振荡试管 D. 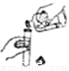 倾倒液体
倾倒液体
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案| 物质 | X | O2 | CO2 | H2O |
| 反应前质量/g | 16 | 70 | 1 | 0 |
| 反应后质量/g | 0 | 待测 | 45 | 36 |
| A. | 该反应为氧化反应 | |
| B. | X中一定只含有碳、氢两种元素 | |
| C. | 表中“待测”值为5 | |
| D. | 反应生成的CO2和H2O的质量比为45:36 |
下列除杂的实验方案中能达到实验目的是的:
方案 | 实验目的 | 实验设计 |
A | 除去氯化钾中的氧酸钾 | 加二氧化猛混合加热 |
B | 除去CO2中的CO | 通过灼热的CuO |
C | 除去氧化铜中的木碳粉 | 隔绝空气加强热 |
D | 除去硝酸铜中的硝酸根 | 加过量锌粉,充分反应后过滤 |
A. A B. B C. C D. D
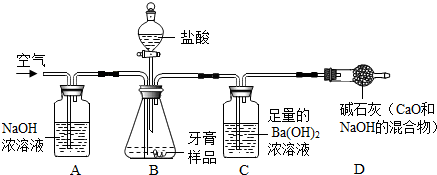
下水道堵塞是日常生活中经常遇到的问题,“管道通”可使堵塞的管道畅通无阻。某同学对此很好奇,于是想探究“管道通”中物质的成分。请一起探究:

【提出问题】“管道通”中的物质是什么?
【查阅资料】
(1)下水管里的淤积物主要为油污、食物残渣、毛发等。
(2)氢氧化钠是强碱,能去除油污,腐蚀毛发一类的东西,常用于疏通管道。
(3)铝粉呈银灰色。
铝与酸、强碱溶液都能反应放出氢气,同时放出大量热。
①铝与盐酸反应的化学方程式________________。
②铝与氢氧化钠溶液反应的化学方程式是2Al+2NaOH+_____═2NaAlO2+3H2↑
【猜想与验证】打开一盒“管道通”,内有一袋白色固体颗粒和一袋银灰色粉末。
(1)猜想:银灰色粉末为铝粉。
实验:取该粉末分别置于两支洁净的试管中,向一只试管中滴加稀盐酸,另一只中滴加__溶液,都产生大量气泡且试管外壁温度明显升高,点燃反应产生的气体火焰呈淡蓝色。
结论:银灰色粉末为铝粉。
(2)猜想:白色固体颗粒为氢氧化钠。
实验操作 | 实验现象 |
①将几粒白色颗粒放在玻璃片上,放置一会儿。 | 白色颗粒潮解 |
②将几粒白色颗粒放入盛有少量水的试管中,并用手触摸试管外壁。 | ____ |
③向步骤②得到的溶液中放入一段羊毛线,加热一段时间。 | 羊毛线逐渐消失 |
结论:白色固体颗粒为氢氧化钠。
【应用】(1)使用“管道通”时,先将银灰色粉状固体添加入被堵塞的管道中,再加入白色固体颗粒,倒入一杯水,堵上管道口。管道内可能出现的现象是____。(填序号)
A.管道内温度明显升高 B.产生大量气体
C.管道被疏通 D.气体燃烧后,火焰成淡蓝色
(2)该“管道通”中的两种物质必须分开保存的原因_______________________________,
该“管道通”必须密封保存的原因(用方程式表示)________________、_________________。
 硒被誉为“抗癌大王”.安徽石台县大山村是全国有名的长寿村,经检测,这是一个全国罕见的富硒区.根据右图提供的硒的有关信息,右图是硒元素在周期表中的相关信息,下列说法不正确的是( )
硒被誉为“抗癌大王”.安徽石台县大山村是全国有名的长寿村,经检测,这是一个全国罕见的富硒区.根据右图提供的硒的有关信息,右图是硒元素在周期表中的相关信息,下列说法不正确的是( )| A. | 硒原子的核内质子数为34 | B. | 硒元素的相对原子质量为78.96 | ||
| C. | 硒的原子结构示意图中x=4 | D. | 该元素位于元素周期表的第四周期 |