题目内容
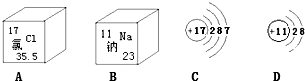
5.如图表示治理汽车尾气所涉及反应的微观过程.下列说法不正确的是( )
| A. | 图中所示单质的化学式为N2 | |
| B. | 生成的单质与化合物的质量比为7:11 | |
| C. | 反应后分子个数变少了 | |
| D. | 图中所示有三种氧化物的分子 |
分析 反应前的四个分子为两种分子,其一为1个C原子和1个O原子构成的CO分子,另一分子为1个N原子和1个O原子构成的NO分子;反应后生成三个分子也为两种分子,一是2个N原子构成的N2分子,另一为1个C原子和2个O原子构成的CO2分子;反应的化学方程式为:2CO+2NO═N2+2CO2;根据反应的化学方程式,判断所列出的四种说法的正误.
解答 解:由治理汽车尾气所涉及反应的微观过程可知,该反应的化学方程式是:2CO+2NO═N2+2CO2.
A、反应中单质只有氮气,其化学式为N2,故A正确;
B、根据反应的化学方程式2CO+2NO═N2+2CO2可知,生成单质与化合物的质量比=28:(44×2)=7:22,故B错误;
C、由方程式可知,每4个分子参加反应,生成了3个分子,反应后分子个数变少了,故C正确;
D、由方程式可知,图中所示有CO、NO、CO2三种氧化物的分子,故D正确.
故选B.
点评 本题的解决思路:利用微观示意图写出反应的化学方程式,然后利用反应的化学方程式解决所提出的问题.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
15.证据是科学探究中获得结论的最重要的依据.让我们一起经历一次寻找证据的旅程吧.
【实验目的】制取纯净的硫酸钡
【反应原理】Na2SO4+BaCl2═BaSO4↓+2NaCl
【实验步骤】取一定量的硫酸钠和氯化钡溶液反应,过滤、洗涤、干燥得到纯净的硫酸钡.
(1)实验中,能直接观察到说明硫酸钠和氯化钡溶液发生化学反应的证据是:有白色沉淀生成.
(2)判断任一反应物是否完全反应的证据可按如下方法获取:
【实验目的】制取纯净的硫酸钡
【反应原理】Na2SO4+BaCl2═BaSO4↓+2NaCl
【实验步骤】取一定量的硫酸钠和氯化钡溶液反应,过滤、洗涤、干燥得到纯净的硫酸钡.
(1)实验中,能直接观察到说明硫酸钠和氯化钡溶液发生化学反应的证据是:有白色沉淀生成.
(2)判断任一反应物是否完全反应的证据可按如下方法获取:
| 猜想 | 方案 | 证据 | 结论 |
| 氯化钡可能已 完全反应 | 取少量滤液,加入稀硫酸 溶液,观察现象 | 无白色沉淀生成 | 氯化钡已完全反应 |
| 硫酸钠可能已 完全反应 | 取少量滤液,加入氯化钡溶液,观察现象 | 无白色沉淀生成 | 硫酸钠未完全反应 |
13.下列物质敞口放置在空气中较长时间后,质量会增加且没有生成新物质的是( )
| A. | 浓硫酸 | B. | 浓盐酸 | C. | 烧碱 | D. | 生石灰 |
20.如图为甲、乙、丙三种物质的溶解度曲线.下列说法正确的是( )
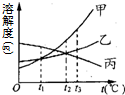

| A. | 在t1℃时,溶解度甲=乙<丙 | |
| B. | 从乙饱和溶液中析出较多量的晶体通常可采用降温结晶法 | |
| C. | 等质量的甲、乙饱和溶液从t3℃降温到t1℃,析出晶体(无结晶水)的质量甲>乙 | |
| D. | t2℃时,将乙、丙的饱和溶液升温至t3℃,乙溶液的溶质质量分数增大,丙溶液的溶质质量分数减小 |
10.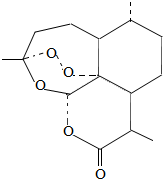 2015年10月,屠呦呦因发现青蒿素治疗疟疾的新疗法获诺贝尔生理学或医学奖.关于青蒿素(化学式为Cl5H22O5)的说法正确的是( )
2015年10月,屠呦呦因发现青蒿素治疗疟疾的新疗法获诺贝尔生理学或医学奖.关于青蒿素(化学式为Cl5H22O5)的说法正确的是( )
 2015年10月,屠呦呦因发现青蒿素治疗疟疾的新疗法获诺贝尔生理学或医学奖.关于青蒿素(化学式为Cl5H22O5)的说法正确的是( )
2015年10月,屠呦呦因发现青蒿素治疗疟疾的新疗法获诺贝尔生理学或医学奖.关于青蒿素(化学式为Cl5H22O5)的说法正确的是( )| A. | 青蒿素由C、H、O三种原子构成 | |
| B. | 28.2g青蒿素中含碳元素的质量为18g | |
| C. | 一个青蒿素分子含有11个氢分子 | |
| D. | C、H、0三种元素的质量比为15:22:5 |
 碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小红同学设计实验对碳酸氢钠的性质进行了探究.请你参与她的探究活动.
碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小红同学设计实验对碳酸氢钠的性质进行了探究.请你参与她的探究活动.