题目内容
6.对于物质微观构成和元素组成的了解,有助于对物质结构、性质、用途的认识.(1)如图是表示气体分子的示意图,图中“
 ”和“
”和“ ”分别表示两种不同的原子.
”分别表示两种不同的原子.
①属于单质的有A,②属于混合物的有BD.
(2)用微粒的观点解释下列问题:
①保持水的化学性质的微粒是:H2O分子.
②同学们上课期间经常能闻到食堂饭菜的香味:分子在不断运动.
(3)将3g的某物质在氧气中充分燃烧生成8.8gCO2和5.4gH2O,由此可以推断该物质的组成的说法中正确的有哪些?( )
A.只含有C、H两种元素 B.可能含有氧元素 C.一定含有氧元素 D.氢元素的质量分数为20%
分析 (1)只要是由分子构成的物质中,如果由一种分子构成,属于纯净物,由两种或两种以上分子构成属于混合物,由一种分子构成的物质中如果由不同元素组成属于化合物.
(2)根据分子的定义和性质解答,分子是保持物质化学性质的一种粒子,它在不断的运动,分子间有间隔,在发生化学变化时,构成物质的分子发生改变,分解成原子,原子再重新组合.
(3)根据可燃物完全燃烧时,其中碳元素全部转变为二氧化碳、氢元素全部转变成水的燃烧规律,由生成的二氧化碳和水中碳、氢元素质量和与可燃物质量进行对比,从而确定该物质的组成元素.
解答 解:(1)A、C图示中都只由一种分子构成,都属于纯净物,其中A中由一种原子构成,属于单质.B、D图示中都至少有两种分子构成,都属于混合物;
故答案为:A;BD;
(2)①水是由水分子构成的,故保持水的化学性质的微粒是水分子.
②同学们上课期间经常能闻到食堂饭菜的香味,说明饭菜的香味的分子是不断运动的,与人的嗅觉细胞接触,而闻到味.
故答案是:①H2O分子;②分子在不断运动;
(3)解:8.8g二氧化碳中所含碳元素的质量=8.8g×$\frac{12}{44}$×100%=2.4g;5.4g水中所含氢元素的质量=5.4g×$\frac{2}{18}$×100%=0.6g;生成物8.8g二氧化碳和5.4g水所含碳、氢元素的质量和=2.4g+0.6g=3g,根据质量守恒定律,则3g某物质中只含碳、氢两种元素,一定不含氧元素.某物质中氢元素的质量分数为$\frac{0.6g}{3g}$×100%=20%.
故选:AD.
点评 本题考查了由一种分子构成的物质属于纯净物,由多种分子构成属于混合物;还考查了有关质量守恒定律、化学式的计算,难度稍大,关键是根据质量守恒定律确定确定物质的元素组成.

 中考解读考点精练系列答案
中考解读考点精练系列答案| A. | 硫 | B. | 碳 | C. | 铁 | D. | 磷 |
| A. | 铁部分锈蚀后没有回收价值 | |
| B. | 铁是地壳中含量第二的金属元素 | |
| C. | 铁生锈,产生的铁锈能阻止铁继续被锈蚀 | |
| D. | 铁生锈是铁只与氧气发生复杂化学反应的过程 |
| A. | 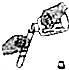 倾倒液体 | B. |  读取液体体积 | C. | 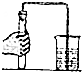 检查气密性 | D. | 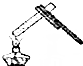 加热液体 |
| 选项 | A | B | C | D |
| 区分的物质 | 苏打和小苏打 | 硝酸铵和硫酸钾 | 黄金和假黄金 (铜锌合金) | 黑醋和酱油 |
| 第一方案 | 分别加水 | 分别与熟石灰研磨闻气味 | 观察颜色 | 闻气味 |
| 第二方案 | 分别加入稀盐酸 | 分别加水制成溶液,触摸容器外壁 | 取样,分别加入硫酸铜溶液 | 观察颜色 |
| A. | A | B. | B | C. | C | D. | D |
 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小李很感兴趣,于是,他和同学们进行探究.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小李很感兴趣,于是,他和同学们进行探究.