题目内容
16.对于碘缺乏疾病的防治措施主要是在食盐中加碘,这里的“碘”应理解为( )| A. | 元素 | B. | 分子 | C. | 原子 | D. | 离子 |
分析 食品、药品、营养品、矿泉水等物质中的“碘”等不是以单质、分子、原子、离子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述.
解答 解:对于碘缺乏疾病的防治措施主要是在食盐中加碘,这里的“碘”等不是以单质、分子、原子、离子等形式存在,这里所指的“碘”是强调存在的元素,与具体形态无关.
故选:A.
点评 本题难度不大,主要考查元素与微观粒子及物质的区别,加深对元素概念的理解是正确解答此类试题的关键.

练习册系列答案
相关题目
5.我市许多建筑遭受白蚁危害.白蚁分泌的蚁酸是一种酸,它能腐蚀很多建筑材料.下列材料,不易被蚁酸腐蚀的是( )
| A. | 大理石 | B. | 钢筋 | C. | 铝合金 | D. | 铜导线 |
20.对实验中的一些做法,分析正确的是( )
| A. | 将粗盐颗粒研磨有利于加快过滤的速度 | |
| B. | 溶解时,为了使粗盐中的氯化钠完全溶解,加的水越多越好 | |
| C. | 蒸发时,玻璃棒起到搅拌、防止液体飞溅的作用 | |
| D. | 蒸发滤液时,待蒸发皿中的滤液蒸干后停止加热 |
6.金属镁广泛应用于火箭、导弹和飞机制造业.从海水或卤水中提取镁的流程如图所示,下列说法中错误的是( )


| A. | 流程Ⅰ中试剂①可使用石灰乳,成本较低 | |
| B. | 流程Ⅰ、Ⅱ的主要目的是将海水或卤水中的氧化镁富集起来,提纯氯化镁 | |
| C. | 流程Ⅱ涉及的化学反应的微观实质是H+和HO-反应生成了H2O | |
| D. | 流程Ⅲ将化学能转化为电能 |
3.下列物质属于纯净物的是( )
| A. | 洁净的空气 | B. | 雪碧饮料 | C. | 加铁酱油 | D. | 二氧化碳 |
4.如表是氯化钠和硝酸钾在不同温度时的溶解度,根据此表回答:
(1)以上两种物质溶解度变化受温度影响较小的是氯化钠
(2)若要比较KNO3与 NaCl在水中的溶解能力,需要控制的变量是水的质量和温度;
(3)若将上表数据在坐标系中绘制成NaCl和KNO3的溶解度曲线,两条曲线的交点对应的温度范围是A.
A.20℃~30℃B.30℃~40℃C.40℃~50℃D.50℃~60℃
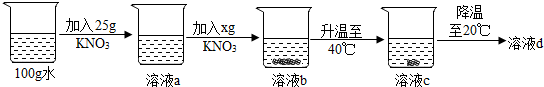
(4)20℃时某同学进行了如下实验,溶液a的质量分数是20%,在此过程中一定是饱和溶液的是bc(填溶液编号),x的取值范围是x>38.9.
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | |
| 溶解度 (g/100g水) | NaCl | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
(2)若要比较KNO3与 NaCl在水中的溶解能力,需要控制的变量是水的质量和温度;
(3)若将上表数据在坐标系中绘制成NaCl和KNO3的溶解度曲线,两条曲线的交点对应的温度范围是A.
A.20℃~30℃B.30℃~40℃C.40℃~50℃D.50℃~60℃
(4)20℃时某同学进行了如下实验,溶液a的质量分数是20%,在此过程中一定是饱和溶液的是bc(填溶液编号),x的取值范围是x>38.9.

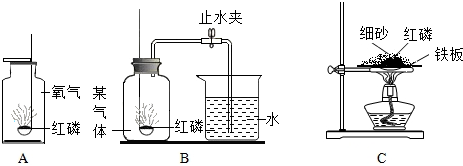
 如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.
如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.