题目内容
9.有一包固体粉末可能含有Na2CO3、FeCl3、CaCl2、NaOH中的一种或几种,为了探究它们的成分,进行如下实验:①取少量该固体粉末加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液;②向滤液中滴加酚酞溶液,溶液变红.根据上述实验回答下列问题:(1)粉末中一定不含FeCl3,一定含有Na2CO3、CaCl2.
(2)为了确定可能含有的物质,取少量②中红色溶液于试管中,加入过量的氯化钙或氯化钡溶液,若溶液仍为红色,则证明该物质一定存在.
分析 根据Na2CO3、FeCl3、CaCl2、NaOH中氯化铁的溶液为黄色,与其它物质间反应生成的沉淀也是有色的沉淀,故依据反应的现象可知固体中一定不会含有氯化铁,由①中会生成白色沉淀,所以一定存在Na2CO3、CaCl2(CaCl2能与碳酸钠反应生成白色沉淀),由②知向滤液中滴加酚酞溶液,溶液变红,所以可能含有氢氧化钠,或含有过量的碳酸钠,进行分析.
解答 解:根据Na2CO3、FeCl3、CaCl2、NaOH中氯化铁的溶液为黄色,与其它物质间反应生成的沉淀也是有色的沉淀,故依据反应的现象可知固体中一定不会含有氯化铁,由①中会生成白色沉淀,所以一定存在Na2CO3、CaCl2(CaCl2能与碳酸钠反应生成白色沉淀),由②知向滤液中滴加酚酞溶液,溶液变红,所以可能含有氢氧化钠,则:
(1)粉末中一定不含FeCl3,一定含有Na2CO3、CaCl2.
(2)为了确定可能含有的物质氢氧化钠,取少量②中红色溶液于试管中,加入过量的氯化钙或氯化钡溶液,若溶液仍为红色,则证明该物质一定存在.
故答案为:
(1)FeCl3,Na2CO3、CaCl2.(2)氯化钙或氯化钡.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
相关题目
19.下列生活中常见的变化中,均属于化学变化的一组是( )
| A. | 干冰升华,钢铁生锈 | B. | 葡萄酿酒,烟花燃放 | ||
| C. | 玻璃破碎,水分蒸发 | D. | 汽油挥发,云消雾散 |
17.下列各组物质的俗称、化学式,用途不一致的是( )
| A. | 生石灰 CaO 做干燥剂 | |
| B. | 纯碱 NaOH 治疗胃酸过多 | |
| C. | 小苏打 NaHCO3 发酵粉主要成分之一 | |
| D. | 干冰 CO2 人工降雨 |
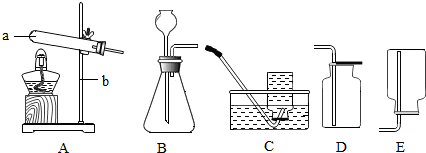
16.用如图装置进行实验,能达到实验目的是( )
| A. | 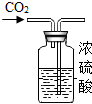 干燥C02 | B. | 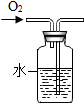 监控02流速 | C. | 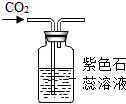 验证CO2性质 | D. | 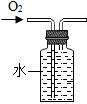 收集O2 |
17.化学课上,老师带来一包白色粉末状漂白剂进行探究.老师介绍它可能是双氧水(H2O2)、过氧碳酸钠和过氧化钙(CaO2)中的一种.
【提出猜想】小科认为该漂白剂肯定不是双氧水,他的理由是双氧水常温下是液态;
【查阅资料】
(1)过氧碳酸钠是一种白色结晶颗粒,易溶于水,并与水反应生成碳酸钠和过氧化氢;
(2)过氧化钙,白色固体,极微溶于水,与水反应缓慢释放氧气,同时生成氢氧化钙,反应的化学方程式为2CaO2+2H2O=2Ca(OH)2+O2↑;
【实验验证】同学们设计了下列实验方案进行验证,请将方案的空格填写完整.
【交流反思】
(1)小刚认为只根据操作①便可确定白色固体的成分,理由是溶液浑浊,说明该漂白剂难溶于水,而过氧化钙难溶于水,过碳酸钠能溶于水,说明该漂白剂是过氧化钙;
(2)小强欲验证该漂白剂与水反应生成的气体为氧气,他的实验方法为取漂白剂于试管中加入适量水,并加入二氧化锰,将带火星的木条伸入试管中若木条复燃,证明该气体是氧气.
【提出猜想】小科认为该漂白剂肯定不是双氧水,他的理由是双氧水常温下是液态;
【查阅资料】
(1)过氧碳酸钠是一种白色结晶颗粒,易溶于水,并与水反应生成碳酸钠和过氧化氢;
(2)过氧化钙,白色固体,极微溶于水,与水反应缓慢释放氧气,同时生成氢氧化钙,反应的化学方程式为2CaO2+2H2O=2Ca(OH)2+O2↑;
【实验验证】同学们设计了下列实验方案进行验证,请将方案的空格填写完整.
| 实验内容 | 实验现象 | 实验结论或解释 |
| ①取3g白色固体放入试管中,加入50ml水中,充分振荡 | 液体浑浊 | \ |
| ②小吴另取少量操作①中的上层清液于试管中,通入二氧化碳 | 有白色沉淀产生 | 该漂白剂的成分是过氧化钙 |
(1)小刚认为只根据操作①便可确定白色固体的成分,理由是溶液浑浊,说明该漂白剂难溶于水,而过氧化钙难溶于水,过碳酸钠能溶于水,说明该漂白剂是过氧化钙;
(2)小强欲验证该漂白剂与水反应生成的气体为氧气,他的实验方法为取漂白剂于试管中加入适量水,并加入二氧化锰,将带火星的木条伸入试管中若木条复燃,证明该气体是氧气.