题目内容
2013年6月,“神舟十号”飞船的顺利升空极大地鼓舞了国人.飞船升空携带了大量的燃料.假设其中某个燃料舱中有肼(N2H4)和四氧化二氮(N2O4)的混合物1300kg,它们反应生成水和氮气,化学方程式为2N2H4+N2O4
3N2+4H2O,则理论上携带四氧化二氮约为( )
| ||
| A、767kg |
| B、535kg |
| C、331kg |
| D、969kg |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:由题意,某个燃料舱中有肼(N2H4)和四氧化二氮(N2O4)的混合物1300kg,它们反应生成水和氮气,由参加反应的肼和四氧化二氮的质量比,计算出理论上携带四氧化二氮的质量即可.
解答:解:由题意,某个燃料舱中有肼(N2H4)和四氧化二氮(N2O4)的混合物1300kg,它们反应生成水和氮气.
2N2H4+N2O4
3N2+4H2O
64 92
肼(N2H4)和四氧化二氮(N2O4)的混合物1300kg,则理论上携带四氧化二氮约为1300kg×
≈767kg.
故选:A.
2N2H4+N2O4
| ||
64 92
肼(N2H4)和四氧化二氮(N2O4)的混合物1300kg,则理论上携带四氧化二氮约为1300kg×
| 92 |
| 64+92 |
故选:A.
点评:本题难度不大,掌握化学反应中各物质之间的质量比等于相对分子质量和的比是正确解答本题的关键.

练习册系列答案
相关题目
如图由两种化合物组成的混合物是(圆圈和黑点表示不同的原子)( )
A、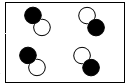 |
B、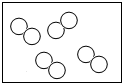 |
C、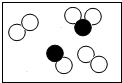 |
D、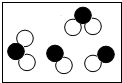 |
下列化学用语既能表示一种元素,又能表示一种原子,还能表示一种物质的是( )
| A、H | B、Mg |
| C、N2 | D、CO |
下列变化中,有一种变化与其它三种变化有本质区别,这种变化是( )
| A、牛奶变质 | B、水结成冰 |
| C、轮胎爆炸 | D、打碎玻璃 |
下列关于水的说法不正确的是( )
| A、水是由2个氢元素、1个氧元素组成的 |
| B、水分子中H、O原子个数比是2:1 |
C、右图是我国的节水标志 |
| D、运用化学方法,可以进行污水处理,实现水资源的重新利用 |