题目内容
11.2014年8月3日,云南省昭通市鲁甸县境内发生6.5级地震,为防止地震灾区的病菌传播,防疫人员大量使用了“漂白粉”来杀菌消毒,“漂白粉”的有效成分为次氯酸钙[化学式为:Ca(ClO)2].试求:(1)次氯酸钙中钙、氧、氯三种元素的原子个数比;
(2)次氯酸钙中钙、氧、氯三种元素的质量比;
(3)次氯酸钙中氯元素的质量分数(精确到0.1%)
(4)若灾区饮用水每50kg至少需要漂白粉250g,则消毒一桶水(约20kg)至少需要加漂白粉的质量.
分析 (1)根据次氯酸钙分子的构成分析;
(2)化合物中各元素质量比=各原子的相对原子质量×原子个数之比进行分析;
(3)利用组成元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,由次氯酸钙的化学式可计算其中钙元素的质量分数;
(4)根据每50kg饮用水至少需要漂白粉250g的质量关系,判断消毒20kg的一桶水需要漂白粉的质量.
解答 解:(1)一个次氯酸钙分子是由1个钙原子、2个氯原子和2个氧原子构成的,则次氯酸钙中钙、氯、氧三种原子个数比为1:2:2;
故答案为:1:2:2;
(2)钙、氯、氧三种元素的质量比=40:(35.5×2):(16×2)=40:71:32;
故答案为:40:71:32;
(3)次氯酸钙中氯元素的质量分数=$\frac{35.5×2}{40+35.5×2+16×2}$×100%≈49.7%,
故答案为:49.7%;
(4)饮用水每50kg至少需要漂白粉250g,则消毒一桶水(约20kg)至少须加漂白粉=$\frac{20kg}{50kg}×250g$=100g
故答案为:100.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
18.下列实验操作中,正确的是(( )
| A. | 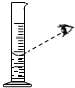 读液体体积 | B. |  倾倒液体 倾倒液体 | C. | 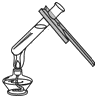 液体的加热 | D. | 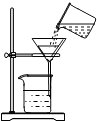 过滤 |
2.有四种失去标签的溶液,它们是:①KCl、②Ba(NO3)2、③AgNO3、④FeCl3,不另加试剂,只用它们相互反应加以鉴别,鉴别出的先后顺序是( )
| A. | ①②③④ | B. | ④③②① | C. | ④③①② | D. | ③①④② |
19.下列物质属于混合物的是( )
| A. | 自来水 | B. | 高锰酸钾 | C. | 过氧化氢 | D. | 金刚石 |
1.日常生活中不可能观察到的现象是( )
| A. | 粗盐久置在空气中会潮解 | |
| B. | 盛有食醋的瓶子打破后,会散发出一种刺激性气味 | |
| C. | 装满水的玻璃瓶结冰后,瓶子炸裂 | |
| D. | 温度和溶剂量不变,久置的食盐水中产生了食盐晶体 |

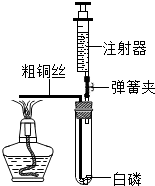 注射器是一种普通的医疗器械,但它在化学实验中发挥着越来越大的作用.某化学兴趣小组为了测定空气中氧气的含量,进行了如下探究活动:
注射器是一种普通的医疗器械,但它在化学实验中发挥着越来越大的作用.某化学兴趣小组为了测定空气中氧气的含量,进行了如下探究活动: