题目内容
9.如表为元素周期表中部分元素的原子结构示意图.请回答下列问题:| 元素名称 | 钠 | 镁 | 铝 | 硅 | 磷 | 硫 | 氯 | 氩 |
| 元素符号 | Na | Mg | Al | Si | P | S | Cl | Ar |
| 原子结构示意图 | 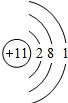 | 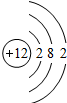 | 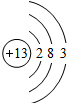 | 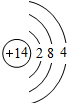 | 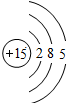 | 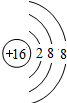 | 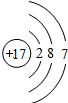 | 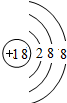 |
(2)表中具有相对稳定结构的元素是Ar.
(3)在化学反应中,每个铝原子易失去3个电子后形成阳离子(填“阳离子”或“阴离子”).
(4)磷元素与氧元素形成化合物的化学式为P2O5.
分析 (1)根据原子中质子数=核外电子数,进行分析解答.
(2)最外层具有8个电子的原子具有相对稳定结构.
(3)最外层电子数<4,则一般为金属元素,在化学反应中易失去电子,据此进行分析解答.
(4)磷元素与氧元素形成化合物是五氧化二磷.
解答 解:(1)原子中质子数=核外电子数,则磷原子的核电荷数x=2+8+5=15.
(2)最外层具有8个电子的原子具有相对稳定结构,表中具有相对稳定结构的元素氩元素,其元素符号为:Ar.
(3)铝原子的最外层电子数为3,在化学反应中,每个铝原子失去3个电子形成铝离子.
(4)磷元素显+5价,氧元素显-2价,两者形成化合物的化学式为P2O5.
故答案为:(1)15;(2)Ar;(3)3;阳离子;(4)P2O5.
点评 本题难度不大,灵活运用元素周期表中元素的信息、原子结构示意图的含义是正确解答本题的关键.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
20.下列各组物质按单质、氧化物、混合物顺序排列的是( )
| A. | 氧气、水、空气 | B. | 氮气、氯酸钾、蔗糖水 | ||
| C. | 铁粉、氨气、石灰石 | D. | 氢气、干冰、冰水混合物 |
17.对于水受热变为水蒸气的现象,下列解释正确的是( )
| A. | 分子之间间隙改变 | B. | 分子大小发生变化 | ||
| C. | 分子的数目增加 | D. | 分子本身发生改变 |
4.“冰毒”是毒性极强的毒品之一,其化学式为C10H15N,下列有关冰毒的说法错误的是( )
| A. | 一个冰毒分子由10个碳原子、15个氢原子、1个氮原子构成 | |
| B. | 冰毒的相对分子质量是149 | |
| C. | 冰毒在空气中完全燃烧只生成CO2和H2O | |
| D. | 冰毒中碳、氢元素的质量比为8:1 |
14.下列物质的用途与性质不能对应的是( )
| A. | 用食醋去除水垢--食醋具有酸性 | |
| B. | 干冰可用做制冷剂--干冰升华吸热 | |
| C. | 氧气用于气焊--氧气具有可燃性 | |
| D. | 稀有气体在通电时发出不同颜色的光 |
1.用实验探究Al和Cu的金属活动性强弱,若提供的试剂只有:CuCl2溶液、AlCl3溶液、稀盐酸和Al、Cu,对此下列说法正确的是( )
| A. | 选用两种合适的试剂即可实现实验目的 | |
| B. | 最多只能设计一种实验方案 | |
| C. | AlCl3溶液加入Cu不能探究金属活动性强弱 | |
| D. | CuCl2溶液时不可或缺的试剂 |
18.以下实验基本操作正确的是( )
| A. | 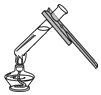 加热液体 | B. | 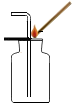 二氧化碳验满 | C. | 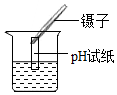 测定溶液酸碱度 | D. | 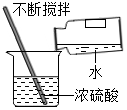 稀释浓硫酸 |
16.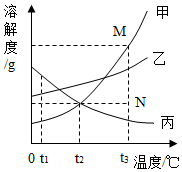 图是甲、乙、丙三种固体物质的溶解度曲线.下列叙述错误的是( )
图是甲、乙、丙三种固体物质的溶解度曲线.下列叙述错误的是( )
 图是甲、乙、丙三种固体物质的溶解度曲线.下列叙述错误的是( )
图是甲、乙、丙三种固体物质的溶解度曲线.下列叙述错误的是( )| A. | t2℃时,三种物质的溶解度大小顺序为:乙>甲=丙 | |
| B. | t2℃时,甲、丙两种物质的溶液中溶质的质量分数相等 | |
| C. | 若甲物质中混有少量的乙物质,可用降温结晶的方法提纯甲 | |
| D. | 采用降低温度的方法,可将饱和的丙物质溶液变成不饱和 |