题目内容
【题目】如图所示是实验室制取气体的常用装置,请回答有关问题. 
(1)用A装置分解KMnO4制取O2时,为了防止制备装置中的固体随气流进入收集装置中,通常采取的措施是 . D装置收集的O2和用C装置收集的O2相比的优点有 .
(2)用B装置制取CO2的反应原理是 .
【答案】
(1)在试管口放一团棉花;纯度高
(2)CaCO3+2HCl═CaCl2+CO2↑+H2O
【解析】解:(1)加热高锰酸钾制取氧气时,为了防止高锰酸钾颗粒随气流进入收集装置中,需要在在试管口放置一棉花团;排水法收集的氧气比较纯净,向上排空气法来收集的氧气比较干燥;故填:在试管口放一团棉花;纯度高;(2)实验室制取二氧化碳用大理石和稀盐酸反应生成氯化钙、水和二氧化碳,方程式是:CaCO3+2HCl═CaCl2+CO2↑+H2O;故填:CaCO3+2HCl═CaCl2+CO2↑+H2O.
【考点精析】通过灵活运用制取氧气的操作步骤和注意点,掌握制取氧气的操作步骤(以高锰酸钾制取氧气并用排水法收集为例)a、步骤:查—装—定—点—收—移—熄即可以解答此题.

 阅读快车系列答案
阅读快车系列答案【题目】下列三套装置(见如图)都可用于实验室制取CO2 . 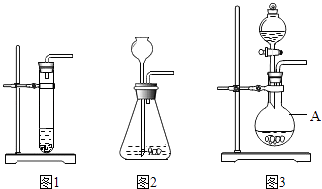
(1)写出实验室制取CO2的化学方程式;
(2)仪器A的名称是;
(3)利用图2装置制取CO2时,长颈漏斗的下端管口必须浸没在溶液中,理由是;
(4)图1和图3装置相比,利用图1装置来制取CO2时,主要不足是(写出一点即可);
(5)化学兴趣小组为了测定石灰石样品中碳酸钙的质量分数,取一定质量的石灰石样品,将20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余成分既不与盐酸反应,也不溶于水),充分反应后经过过滤、干燥等操作,最后称量,得实验数据如下表:
稀盐酸的用量 | 剩余固体的质量 |
第一次加入5g | 1.5g |
第二次加入5g | 1.0g |
第三次加入5g | 0.5g |
第四次加入5g | 0.3g |
石灰石样品中碳酸钙的质量分数为;
原稀盐酸中溶质的质量分数为多少?(写出计算过程)