题目内容
11.如图是稀盐酸和氢氧化钠溶液反应的pH变化曲线图,据图分析能得出的正确结论是( )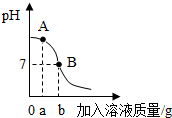
| A. | 该反应是将氢氧化钠溶液中滴入稀盐酸中 | |
| B. | A点时,溶液的溶质为NaOH、NaCl | |
| C. | B点表示参加反应的HCl和NaOH的质量相等 | |
| D. | 最终溶液液的pH一定为0 |
分析 氢氧化钠溶液呈碱性,其pH大于7,盐酸呈酸性,其pH小于7,氢氧化钠溶液和盐酸可以发生中和反应,恰好完全反应时其pH等于7,氢氧化钠过量时显碱性,盐酸过量时显酸性.
解答 解:A、根据图象可以看出,开始时溶液的pH大于7,溶液呈碱性,故是将稀盐酸滴向氢氧化钠溶液中,故错误;
B、从图象可以看出,A点溶液呈碱性,溶液中的溶质有氯化钠和氢氧化钠两种物质,故正确;
C、B点表示氢氧化钠与盐酸恰好完全反应,此时所加的盐酸和氢氧化钠溶液的质量不一定相等,故错误;
D、最终溶液液的pH可能为0,故错误.
答案:B.
点评 本题以图象的形式考查了酸碱中和反应过程中溶液pH的变化,完成此题,要抓住曲线变化的趋势和关键点的意义.

练习册系列答案
相关题目
2.2月26日,备受瞩目的台州市“两会”在椒江剧院隆重开幕,来自全市各条战线的人大代表,政协委员精神抖擞,汇聚一堂,履行宪法和法律赋予的神圣职责,共同绘制台州2013年发展蓝图.而“低碳生活”也成了会议的关键词.“低碳生活”是指减少能源消耗、节约资源,从而降低二氧化碳排放的一种时尚健康的生活方式.下列做法不符合“低碳生活”理念的是( )
| A. | 教科书循环使用 | |
| B. | 多用电子邮箱、QQ等即时通讯工具 | |
| C. | 禁止使用煤、石油、天然气 | |
| D. | 提倡乘坐公共交通工具、骑自行车或步行等出行方式 |
6.分类是学习和研究化学的一种常用的科学方法.下列物质中,属于纯净物的是( )
| A. | 洁净的空气 | B. | 不锈钢钉 | C. | 稀盐酸 | D. | 蒸馏水 |
3.下列各组溶液中,利用无色酚酞试液可以鉴别的是( )
| A. | Ca(OH)2,H2SO4,HCl | B. | NaOH,Ca(OH)2,HCl | ||
| C. | H2SO4,NaOH,Ca(OH)2 | D. | NaCl,NaOH,HCl |
12.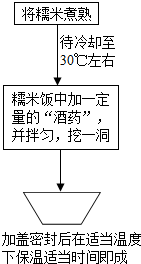 小边同学的家人都喜欢喝酒.奶奶喜欢喝自己酿制的甜米酒,爸爸则常喝点“同山烧酒”.
小边同学的家人都喜欢喝酒.奶奶喜欢喝自己酿制的甜米酒,爸爸则常喝点“同山烧酒”.
(1)如图是奶奶酿造甜米酒的具体操作过程:先将糯米加热煮至七成熟,待冷却至30℃后,加少许的水和一定量的“酒药”(实际是酵母菌菌种)与糯米饭混合后置于一坛内,在糯米饭中央挖一个小洞,加盖密封后,置于适当地方保温28℃,一天后即可食用.奶奶说:“酿甜米酒的关键是保温和密封”.你认为:需要保温和将坛密封的目的是:保温是为酵母菌提供适宜的温度,利于酵母菌的生长、繁殖和发酵;密封的目的是减少与空气的接触,使酵母菌在无氧条件下分解葡萄糖产生酒精.
(2)有一天小边同学把爸爸喝的“同山烧酒”倒了一点在碗里,居然能被点燃,好奇的小边同学在老师的指导下设计实验作如下探究:
①取一定量的“同山烧酒”加入足量的硫酸铜粉末(碱石灰)吸收掉酒中的全部水份.
②将得到的纯酒精和氧气置于一个完全密闭的容器中引燃,反应生成二氧化碳、水蒸气和一种未知气体X,测得反应前后各物质的质量如下表:
则表中m的值为2.8,若要减少x的生成量,应增加氧气(或减少酒精)的量.
 小边同学的家人都喜欢喝酒.奶奶喜欢喝自己酿制的甜米酒,爸爸则常喝点“同山烧酒”.
小边同学的家人都喜欢喝酒.奶奶喜欢喝自己酿制的甜米酒,爸爸则常喝点“同山烧酒”.(1)如图是奶奶酿造甜米酒的具体操作过程:先将糯米加热煮至七成熟,待冷却至30℃后,加少许的水和一定量的“酒药”(实际是酵母菌菌种)与糯米饭混合后置于一坛内,在糯米饭中央挖一个小洞,加盖密封后,置于适当地方保温28℃,一天后即可食用.奶奶说:“酿甜米酒的关键是保温和密封”.你认为:需要保温和将坛密封的目的是:保温是为酵母菌提供适宜的温度,利于酵母菌的生长、繁殖和发酵;密封的目的是减少与空气的接触,使酵母菌在无氧条件下分解葡萄糖产生酒精.
(2)有一天小边同学把爸爸喝的“同山烧酒”倒了一点在碗里,居然能被点燃,好奇的小边同学在老师的指导下设计实验作如下探究:
①取一定量的“同山烧酒”加入足量的硫酸铜粉末(碱石灰)吸收掉酒中的全部水份.
②将得到的纯酒精和氧气置于一个完全密闭的容器中引燃,反应生成二氧化碳、水蒸气和一种未知气体X,测得反应前后各物质的质量如下表:
| 物质 | 酒精 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 4.6 | 8 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 4.4 | 5.4 | m |
13.室温时将下列各物质加入到一定量的水中不能形成饱和溶液的是( )
| A. | KNO3晶体 | B. | CO2气体 | C. | NaCl晶体 | D. | C2H5OH(酒精) |

