题目内容
9.【提出假设】a.Ti的金属活动性比Mg强;b.Ti的金属活动性介于Mg和Ag之间.
【查阅资料】在相同条件下,金属与酸反应,产生气泡的速率越快,则该金属活动性越强.
【实验设计】同温下,取大小相同的这三种金属薄片,分别投入等体积、等浓度的足量稀盐酸中,观察现象.
请回答:三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是除去表面的附着物.
【实验现象】
| 金属 | Ti | Mg | Ag |
| 反应现象 | 反应缓慢 | 反应强烈 | 无明显现象 |
[结论]用不同浓度的足量稀盐酸反应,是否也能得出同样结论?不能,请说明理由反应速率与反应物浓度有关
(1)小刚与小红分别做相同质量的不同金属与同质量、同质量分数的稀H2SO4反应的实验,实验结束后,分别交上的实验报告,并绘制出金属Zn、Fe分别与稀H2SO4反应放出H2的函数图象(如图所示).
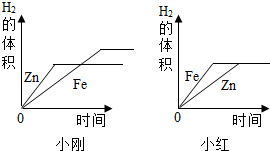
两个图象中存在有错误的是小红的图象,判断错误的理由是Zn的反应速率较Fe快,因此图象中Fe与Zn标反了,
图象不同的原因是小刚取的金属量较少,金属完全反应,而小红取的酸量较少,酸完全反应.
由该实验可以得到的结论:
①金属与酸反应的速率与金属活动性有关.
②金属与酸反应中若生成盐中金属价态相同,则生成的氢气量与相对原子质量有关.
(2)将铁粉加到硫酸铜溶液中,可能观察到的现象有产生红色固体,溶液由蓝色变成浅绿色.
分析 【实验设计】
金属长期暴露在空气中时,可能被空气中的氧气氧化;
【实验结论】
根据实验现象可以判断实验结论;
反应速率和反应物浓度有关,即反应物浓度越大,反应速率越快;
铁和硫酸天反应生成硫酸亚铁和铜.
解答 解:【实验设计】
三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是除去表面的附着物.
故填:除去表面的附着物.
【实验结论】
原假设中a不正确,理由是:Ti和稀盐酸反应不如Mg和稀盐酸反应强烈,因此Ti的金属活动性比Mg弱.
故填:a;Ti的金属活动性比Mg弱.
[结论]
用不同浓度的足量稀盐酸反应,不能得出同样结论,这是因为反应速率与反应物浓度有关.
故填:不能;反应速率与反应物浓度有关.
(1)两个图象中存在有错误的是小红的图象,判断错误的理由是Zn的反应速率较Fe快,因此图象中Fe与Zn标反了;
图象不同的原因是:小刚取的金属量较少,金属完全反应,而小红取的酸量较少,酸完全反应.
故填:小红;Zn的反应速率较Fe快,因此图象中Fe与Zn标反了;小刚取的金属量较少,金属完全反应,而小红取的酸量较少,酸完全反应.
①金属与酸反应的速率与金属活动性有关.
故填:金属活动性.
②金属与酸反应中若生成盐中金属价态相同,则生成的氢气量与相对原子质量有关.
故填:相对原子质量.
(2)将铁粉加到硫酸铜溶液中,可能观察到的现象有产生红色固体,溶液由蓝色变成浅绿色.
故填:产生红色固体,溶液由蓝色变成浅绿色.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20. (1)天然水中含有的部分杂质如表所示:
(1)天然水中含有的部分杂质如表所示:
请根据上表内容回答:
①写出“主要气体”中两种气体的化学式O2、CO2;硫化氢中氢元素的化合价为+1;
②写出“主要离子”中钙离子和硫酸根离子的符号Ca2+、${SO}_{4}^{2-}$;
③写出由“生物生成物”中的离子组合成的一种化合物的化学式NH4H2PO4.
(2)如图是某同学自制的简易净水装置,其中起吸附作用的是活性炭,此过程属于物理变化.
(3)某自来水厂生产的主要步骤为:河水→A(明矾)→B(沉淀)→C(过滤)→D(加液氯)→净水.试回答:
①可以除去较大颗粒、悬浮物杂质的步骤是A,能够消毒杀菌的步骤为D;(填编号)
②明矾的化学式为KAl(SO4)2,其中S元素的化合价为+6;
③生产得到的净水是混合物(填“纯净物”或“混合物”),其原因是净水中还含有其它可溶性物质.
 (1)天然水中含有的部分杂质如表所示:
(1)天然水中含有的部分杂质如表所示:| 溶 解 物 质 | 悬浮物质 | ||
| 主要气体 | 主要离子 | 生物生成物 | 细菌、藻类及原生 物、泥沙、黏土等 |
| 氧气 二氧化碳 硫化氢等 | 钙离子、氯离子、 硫酸根离子、镁离子 | NH4+、NO2-、 HPO42-、Fe3+、 H2PO4-等 | |
①写出“主要气体”中两种气体的化学式O2、CO2;硫化氢中氢元素的化合价为+1;
②写出“主要离子”中钙离子和硫酸根离子的符号Ca2+、${SO}_{4}^{2-}$;
③写出由“生物生成物”中的离子组合成的一种化合物的化学式NH4H2PO4.
(2)如图是某同学自制的简易净水装置,其中起吸附作用的是活性炭,此过程属于物理变化.
(3)某自来水厂生产的主要步骤为:河水→A(明矾)→B(沉淀)→C(过滤)→D(加液氯)→净水.试回答:
①可以除去较大颗粒、悬浮物杂质的步骤是A,能够消毒杀菌的步骤为D;(填编号)
②明矾的化学式为KAl(SO4)2,其中S元素的化合价为+6;
③生产得到的净水是混合物(填“纯净物”或“混合物”),其原因是净水中还含有其它可溶性物质.
17.下列物质中含有氧分子的是( )
| A. | 双氧水(H2O2) | B. | 二氧化硫(SO2) | C. | 二氧化碳(CO2) | D. | 液态空气 |
14.如图所示,某校化学兴趣小组用过氧化氢(H2O2)溶液(MnO2作催化剂)制取干燥的氧气,并用来侧定1Og某铜粉样品(含少量杂质碳)中铜的质量分数.回答下列问题:

(温馨提示:2Cu+O2$\frac{\underline{\;加热\;}}{\;}$2CuO,NaOH溶液可以吸收二氧化碳);
(1)装置A中发生反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.装置B的作用是吸收水蒸气.
(2)通过称量反应前后装置D的质量,进行计算便可求出样品中铜的质量分数.
(3)实验完毕,小兰同学误将用剩的H2O2溶液和装置C玻璃管中的剩余固体一起倒入烧杯中,发现有大量的气泡产生,经检验确认产生的气体是氧气.小刚误和小何两位同学对此颇感兴趣,进而展开了他们的探究之旅.
【提出问题】是哪种物质加快了H2O2的分解速率?
【大胆猜想】猜想Ⅰ:剩余固体中的CuO加快了H2O2溶液的分解.
猜想Ⅱ:剩余固体中的铜加快了H2O2溶液的分解.
猜想Ⅲ:氧化铜能做H202分解的催化剂.
【实验验证】
【讨论交流】小周同学认为,根据实验二得出的两个结论就能判断Ⅲ成立,你是否支持他的观点?并简述理由.
答:不支持.没有证明反应前后物质的化学性质是否改变.

(温馨提示:2Cu+O2$\frac{\underline{\;加热\;}}{\;}$2CuO,NaOH溶液可以吸收二氧化碳);
(1)装置A中发生反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.装置B的作用是吸收水蒸气.
(2)通过称量反应前后装置D的质量,进行计算便可求出样品中铜的质量分数.
(3)实验完毕,小兰同学误将用剩的H2O2溶液和装置C玻璃管中的剩余固体一起倒入烧杯中,发现有大量的气泡产生,经检验确认产生的气体是氧气.小刚误和小何两位同学对此颇感兴趣,进而展开了他们的探究之旅.
【提出问题】是哪种物质加快了H2O2的分解速率?
【大胆猜想】猜想Ⅰ:剩余固体中的CuO加快了H2O2溶液的分解.
猜想Ⅱ:剩余固体中的铜加快了H2O2溶液的分解.
猜想Ⅲ:氧化铜能做H202分解的催化剂.
【实验验证】
| 实验方案 | 实验现象 | 分析及结论 |
| 实验一:将带火星的木条伸入盛有5mL5%H2O2溶液的试管 | 带火星木条不复燃 | H2O2溶液常温下产生氧气的量很少,不足以使带火星的木条复燃 |
| 实验二:向盛有5mL5%H2O2溶液的试管中加入1gCuO固体,将一根带火星的木条伸入试管,观察现象.待反应结束后将试管里的剩余物进行过滤、洗涤、干燥、称量.对比反应前后CuO的质量 | 带火星的木条复燃. 称得固体质量为1g | 猜想Ⅰ成立.反应前后固体的质量相等 |
| 实验三:向盛有5mL5%H2O2溶液的试管中加入1g铜,将带火星的木条伸入试管,观察现象 | 没有气泡产生,带火星木条不复燃 | 猜想Ⅱ不成立(填”成立“或“不成立”) |
答:不支持.没有证明反应前后物质的化学性质是否改变.
19.下列物质由离子构成的是( )
| A. | 铜 | B. | 食盐 | C. | 金刚石 | D. | 氧气 |