题目内容
12.一定质量的CO和CO2的混合气体,通入足量的氢氧化钡溶液中,充分反应后过滤,不溶物与原混合气体的质量恰好相等.则原混合气体中CO和CO2的质量比为153:44.分析 根据反应方程式:Ba(OH)2+CO2=BaCO3↓+H2O,分别设出CO和CO2的质量,利用生成的沉淀质量恰好等于原混合气体的质量的关系,列出等式,进行解答.
解答 解:设混合气体中CO的质量为x,CO2的质量为y
Ba(OH)2 +CO2=BaCO3↓+H2O
44 197
y x+y
$\frac{44}{y}=\frac{197}{x+y}$
x:y=153:44
答案:153:44
点评 由于题中生成的沉淀和所取的混合气体质量相等,该问题的焦点集中到混合气体的质量与反应生成的碳酸杯的质量上,如果有了碳酸钡的质量,一切问题都会迎刃而解.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.氧的相对原子质量是( )
| A. | 16 | B. | 1.6克 | C. | 2.657×10-27 | D. | 16克 |
4.在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后物质质量如下:
处理数据后得出的结论错误的是( )
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 5 | 2 | 20 | 22 |
| 反应后质量/g | 待测 | 11 | 28 | 5 |
| A. | 反应类型为分解反应 | B. | X可能是该反应的催化剂 | ||
| C. | Y、Z变化的质量比是9:8 | D. | 反应后X的质量为0g |
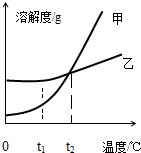
1.如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )

| A. | 甲物质的溶解度一定大于乙物质的溶解度 | |
| B. | 将甲溶液从t2℃降温到t1℃时,一定有晶体析出 | |
| C. | t2℃时,甲、乙饱和溶液的溶质质量分数相等 | |
| D. | 将t2℃时乙的饱和溶液变为不饱和溶液,可采用降温的方法 |

