题目内容
20.下列变化与性质的描述中,前者一定是物理变化,后者一定为化学性质的是(( )| A. | 冰雪融化、光合作用 | B. | 发光放热、食物易腐败 | ||
| C. | 电解水、氢气有可燃性 | D. | 汽油挥发、钢铁易生诱 |
分析 本题考查学生对物理变化和化学变化的确定.判断一个变化是物理变化还是化学变化,要依据在变化过程中有没有生成其他物质,生成其他物质的是化学变化,没有生成其他物质的是物理变化.
解答 解:A、冰雪融化属于物理变化、光合作用属于化学变化,故A错;
B、发光放热可能是物理变化也可能是化学变化、食物易腐败属于化学性质,故B错;
C、电解水属于化学变化、氢气有可燃性属于化学性质,故C错;
D、汽油挥发属于物理变化、钢铁易生锈属于化学性质,故D正确.
故选D.
点评 搞清楚物理变化和化学变化的本质区别是解答本类习题的关键.判断的标准是看在变化中有没有生成其他物质.一般地,物理变化有物质的固、液、气三态变化和物质形状的变化.

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
10.查资料显示,过氧化钠(Na2O2)和二氧化碳反应生成碳酸钠和氧气,化学方程式2Na2O2+2CO2=2Na2CO3+O2.小翔同学和小何同学分别设计了图甲和图乙的实验装置.检查气密性良好后进行实验验证.
预热后对试管进行加热(2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O)
(1)观察到图甲浓硫酸中有气泡产生,蚊香熄灭,浓硫酸的作用是干燥二氧化碳,观察图乙中的现象是蚊香燃烧更剧烈,说明有氧气产生,由资料和实验可得出的结论是湿润的二氧化碳更容易和过氧化钠反应.
(2)某化学兴趣小组对以上甲、乙装置试管中加热后的成分进行探究分析.

[提出问题]加热后的试管中残留物成分是什么呢?
[提出猜想]猜想1:只有碳酸钠 猜想2:只有碳酸氢钠 猜想3:有碳酸钠和碳酸氢钠.
[查阅资料]①碳酸钠固体受热不分解.
②碳酸氢钠溶液中滴加氯化钙溶液无明显现象,而碳酸钠溶液中滴加氯化钙溶液有白色沉淀产生.
[实验探究]
[反思交流]小雯同学认为,不用实验可得出猜想2错误,其理由是碳酸氢钠受热易分解,不可能只含有碳酸氢钠.
预热后对试管进行加热(2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O)
(1)观察到图甲浓硫酸中有气泡产生,蚊香熄灭,浓硫酸的作用是干燥二氧化碳,观察图乙中的现象是蚊香燃烧更剧烈,说明有氧气产生,由资料和实验可得出的结论是湿润的二氧化碳更容易和过氧化钠反应.
(2)某化学兴趣小组对以上甲、乙装置试管中加热后的成分进行探究分析.

[提出问题]加热后的试管中残留物成分是什么呢?
[提出猜想]猜想1:只有碳酸钠 猜想2:只有碳酸氢钠 猜想3:有碳酸钠和碳酸氢钠.
[查阅资料]①碳酸钠固体受热不分解.
②碳酸氢钠溶液中滴加氯化钙溶液无明显现象,而碳酸钠溶液中滴加氯化钙溶液有白色沉淀产生.
[实验探究]
| 实验内容 | 预测现象 | 结论 |
| 实验一:取一定量残留固体于试管中,加热一段时间后,冷却,称量 | 加热前后固体质量减少(“不变”或“减少”). | 含有碳酸氢钠 |
| 实验二:取适量残留固体于试管中,加放蒸馏水充分振荡,滴入氯化钙溶液. | 溶液中产生白色沉淀 | 含有碳酸钠 |
| 结合实验一和实验二得出,猜想3正确. | ||
8. 化学活动课上同学们对金属的性质及合金的成份进行了探究,请你参与.
化学活动课上同学们对金属的性质及合金的成份进行了探究,请你参与.
(1)取等质量的金属,分别加入足量稀硫酸,完成如表四组实验.
①写出实验中一个反应的化学方程式Zn+H2SO4═ZnSO4+H2↑或Mg+H2SO4═MgSO4+H2↑.
②根据表中ACD实验(选填序号),即可判断Mg、Cu、Zn三种金属的活动性顺序.
(2)探究合金的成份,某合金可能由Mg、Cu、Zn、Al四种金属中的两种组成.
[提出问题]合金由哪两种金属组成?
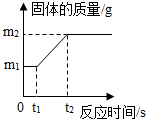
[实验探究]①取该合金m1g,在足量氧气中反应,生成固体质量为m2g,m1和m2的关系如图所示,则(m1-m2)g表示的意义是参加反应的氧气的质量.
②再向m2g的固体中加入稀硫酸,微热,固体全部溶解,得溶液M,继续进行如下实验,补充完成内容.
[分析结论]③若m1=4,m2=7.2,结合上述实验分析,合金的成份是铜和铝.
(3)根据上述实验总结金属的化学性质金属能与酸反应,能与氧气反应,金属还能与某些盐反应.
 化学活动课上同学们对金属的性质及合金的成份进行了探究,请你参与.
化学活动课上同学们对金属的性质及合金的成份进行了探究,请你参与.(1)取等质量的金属,分别加入足量稀硫酸,完成如表四组实验.
| 药品/序号 | A | B | C | D |
| 金属 | 铜粉 | 锌粉 | 锌粉 | 镁粉 |
| 稀硫酸 | 9.8%硫酸 | 19.6%硫酸 | 9.8%硫酸 | 9.8%硫酸 |
②根据表中ACD实验(选填序号),即可判断Mg、Cu、Zn三种金属的活动性顺序.
(2)探究合金的成份,某合金可能由Mg、Cu、Zn、Al四种金属中的两种组成.
[提出问题]合金由哪两种金属组成?
[实验探究]①取该合金m1g,在足量氧气中反应,生成固体质量为m2g,m1和m2的关系如图所示,则(m1-m2)g表示的意义是参加反应的氧气的质量.
②再向m2g的固体中加入稀硫酸,微热,固体全部溶解,得溶液M,继续进行如下实验,补充完成内容.
| 实验操作 | 实验现象 | 结论和化学方程式 |
| 向M中加入ag铁粉、搅拌 | 化学方程式:Fe+CuSO4=FeSO4+Cu Fe+H2SO4═FeSO4+H2↑ M中的溶质:CuSO4、H2SO4 | |
| 过滤,把所得固体洗涤、干燥,称其质量也为ag,并向此固体中加入稀硫酸 | 无明显现象 |
(3)根据上述实验总结金属的化学性质金属能与酸反应,能与氧气反应,金属还能与某些盐反应.
5.如图表示氢气和氧气发生的化学反应,通过该反应得出的信息不正确的是( )


| A. | 该反应是化合反应 | |
| B. | 保持水化学性质的微粒是H2O分子 | |
| C. | 每个水分子是由1个氢分子和1个氧分子构成的 | |
| D. | 在化学变化中分子可分,原子不可分割,只是重新排列组合 |

