题目内容
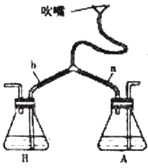
 构建知识网络,可以帮助我们理解知识间的内在联系.如图是盐酸与不同类别物质之间反应的知识网络.
构建知识网络,可以帮助我们理解知识间的内在联系.如图是盐酸与不同类别物质之间反应的知识网络.①图中M应为
②盐酸和氢氧化钠溶液反应的方程式为
③写出用盐酸除铁锈(主要成分Fe2O3)的化学方程式
考点:酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的酸 酸的通性
分析:把盐酸的性质用网络框架的形式表示出来,可以更直观的让学生了解和记忆.根据盐酸的化学性质:(1)跟指示剂反应,(2)跟活泼金属起置换反应,(3)跟碱性氧化物反应,(4)跟某些盐反应,(5)跟碱起中和反应 据此结合盐酸溶液的一些典型反应即可解答本题.
解答:解:①盐酸可与五类物质发生化学反应,图中M应为其中的碱类物质;
②盐酸和氢氧化钠溶液反应的方程式为NaOH+HCl=NaCl+H2O;
③铁锈属于金属氧化物,与盐酸反应生成盐和水,反应中元素的化合价不变,方程式为6HCl+Fe2O3=2FeCl3+3H2O;
故答案为:①碱,②NaOH+HCl=NaCl+H2O,③6HCl+Fe2O3=2FeCl3+3H2O.
②盐酸和氢氧化钠溶液反应的方程式为NaOH+HCl=NaCl+H2O;
③铁锈属于金属氧化物,与盐酸反应生成盐和水,反应中元素的化合价不变,方程式为6HCl+Fe2O3=2FeCl3+3H2O;
故答案为:①碱,②NaOH+HCl=NaCl+H2O,③6HCl+Fe2O3=2FeCl3+3H2O.
点评:盐酸是酸的代表物质,熟记酸的通性是解决此类问题的关键所在,属基础性知识考查题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
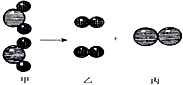
 如图是某化学反应的微观粒子示意图.
如图是某化学反应的微观粒子示意图. B.两个
B.两个 C.一个
C.一个 D.两个
D.两个