题目内容
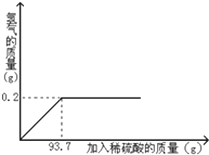 黄铜是铜和锌的合金,可以用来制造机器、电器零件及日用品.为了测定某黄铜样品中铜的质量分数,取20g该样品向其中加入一定量的稀硫酸,恰好完全反应,产生氢气的质量与加入稀硫酸的质量关系如图所示.
黄铜是铜和锌的合金,可以用来制造机器、电器零件及日用品.为了测定某黄铜样品中铜的质量分数,取20g该样品向其中加入一定量的稀硫酸,恰好完全反应,产生氢气的质量与加入稀硫酸的质量关系如图所示.(1)完全反应后,生成H2的质量为
(2)完全反应后所得溶液的溶质质量分数是多少(保留一位小数)?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据图可知氢气的质量.
(2)根据反应的化学方程式结合生成氢气的质量可以计算出反应生成的硫酸锌的质量,然后求出其质量分数即可.
(2)根据反应的化学方程式结合生成氢气的质量可以计算出反应生成的硫酸锌的质量,然后求出其质量分数即可.
解答:解:(1)从图中可以知道生成氢气的质量为0.2;
(2)设锌的质量为x,硫酸锌的质量为y
Zn+H2SO4═ZnSO4+H2↑
65 161 2
x y 0.2g
=
=
解得:x=6.5g y=16.1g
反应后溶液的溶质质量分数═
×100%=16.1%
答:完全反应后所得溶液的溶质质量分数是16.1%.
(2)设锌的质量为x,硫酸锌的质量为y
Zn+H2SO4═ZnSO4+H2↑
65 161 2
x y 0.2g
| 65 |
| x |
| 161 |
| y |
| 2 |
| 0.2g |
解得:x=6.5g y=16.1g
反应后溶液的溶质质量分数═
| 16.1g |
| 6.5g+93.7g-0.2g |
答:完全反应后所得溶液的溶质质量分数是16.1%.
点评:有关反应后所得溶液的计算是初中化学的一个重点,计算溶液质量的方法一般是:所加入的所有物质的质量总和-生成沉淀的质量-生成气体的质量.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目

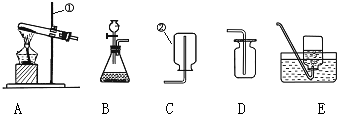
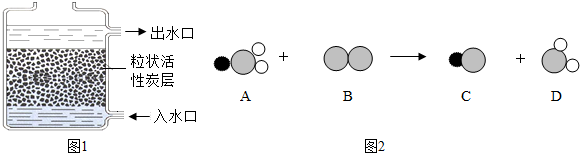
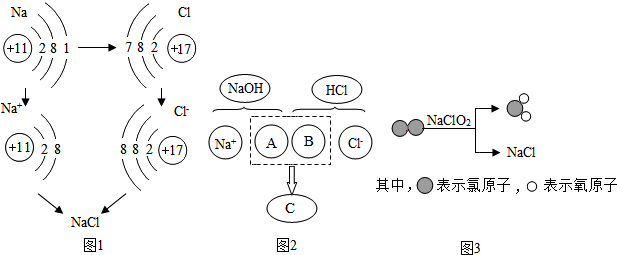
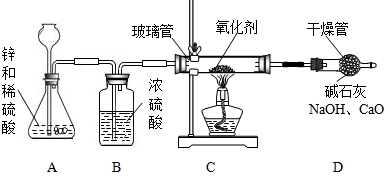 用如图装置及药品进行实验.
用如图装置及药品进行实验.