题目内容
15.请用所学化学知识解释下列原理.(1)洗涤剂能除去油污,是因为它具有乳化功能.
(2)用硫酸除铁锈,其反应现象?反应原理是什么?
(3)用化学方程式表示含Mg(OH)2的药物治疗胃酸过多症的原理.
分析 (1)根据洗涤剂的乳化作用考虑;
(2)根据硫酸除铁锈反应考虑;
(3)根据化学方程式的写法考虑.
解答 解:(1)洗涤剂能除去油污是利用乳化原理将大的油滴颗粒分解成小的油滴微粒,便于用水冲掉;
(2)铁锈的主要成分是氧化铁,能与硫酸反应生成硫酸铁和水,溶液由无色变为黄色,化学方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(3)反应物是氢氧化镁和盐酸,生成物是氯化镁和水,用观察法配平即可.
故答案为:(1)乳化;
(2)溶液由无色变为黄色;Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(3)Mg(OH)2+2HCl═MgCl2+2H2O.
点评 本题考查了化学与生活的知识,完成此题,可以依据题干提供的信息结合已有的知识进行.书写反应的化学方程式要注意配平.

练习册系列答案
相关题目
5.为测定21.2g某变质氢氧化钠的固体中碳酸钠的含量,将其配置成 500g溶液,分别取出50g用两种方法进行测定,已知:Na2CO3+BaCl2═BaCO3↓+2NaCl
请任选1种方法的数据,
(1)计算50g溶液中碳酸钠的质量分数(写出计算过程及结果)
(2)计算该固体中碳酸钠的质量分数(写出计算过程及结果)
| 加入的试剂 | 测得数据 | |
| 方法1 | 足量BaCl2溶液 | BaCO3沉淀1.97g |
| 方法2 | 足量稀硫酸 | CO2气体0.44g |
(1)计算50g溶液中碳酸钠的质量分数(写出计算过程及结果)
(2)计算该固体中碳酸钠的质量分数(写出计算过程及结果)
6.下列有关说法中,正确的是( )
| A. | 室内放置一大盆水,就可防止煤气中毒 | |
| B. | 室内着火,应立即开窗通风 | |
| C. | 夜间室内煤气泄露,立即开灯检查 | |
| D. | 久违开启的菜窖,不可贸然进入 |
10.实验结束后,下列仪器的放置方法正确的是( )
| A. |  | B. | 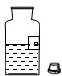 | C. | 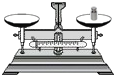 | D. | 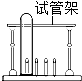 |
20.下列推理正确的是( )
| A. | 单质是由一种元素组成的,所以一种元素只能组成一种单质 | |
| B. | 氧化物中一定含有氧元素,所以含有氧元素的化合物一定是氧化物 | |
| C. | 铝表面的氧化铝薄膜能起保护作用,则铁表面的氧化铁也起保护作用 | |
| D. | 化合物是由不同种元素组成的纯净物,则只含一种元素的物质一定不是化合物 |
1.下列图象不能正确反映对应变化关系的是( )
| A. | 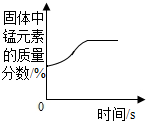 加热一定量的高锰酸钾固体 | |
| B. |  向一定量的过氧化氢溶液中加入二氧化锰,溶液中水的质量与反应时间的关系图 | |
| C. |  将水通电电解一段时间,生成气体的体积随反应时间的变化关系 | |
| D. |  用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气 |
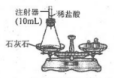 在探究“化学反应前后,物质的总质量是否发生变化”时,老师在课堂上按如图所示演示实验发生反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑
在探究“化学反应前后,物质的总质量是否发生变化”时,老师在课堂上按如图所示演示实验发生反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑