题目内容
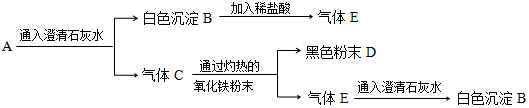
3. 构建模型和构建知识网络是学习化学重要的学习方法,小军同学利用左手构建酸的化学性质知识网络,如图所示(其中A、B表示与酸反应的
构建模型和构建知识网络是学习化学重要的学习方法,小军同学利用左手构建酸的化学性质知识网络,如图所示(其中A、B表示与酸反应的一类物质,D表示生成物),请结合图示回答下列问题:
(1)如用湿润的pH试纸测定盐酸的pH,则结果
会偏大(填“偏大”“偏小”或“无影响”).
(2)图中①的现象是紫色石蕊变红色.
(3)写出一个符合图中④的化学方程式HCl+NaOH=NaCl+H2O.
(4)图中⑤的性质在工业上可用于金属除锈(填用途)
分析 (1)根据用湿润的pH试纸测定盐酸的pH,再蘸取待测液滴在pH试纸上,稀释了待测溶液,使溶液的酸性减弱进行分析;
(2)根据紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝进行分析;
(3)根据④为酸碱中和反应,可以是稀盐酸与氢氧化钠反应生成水和氯化钠进行分析;
(4)根据⑤可能稀盐酸与铁锈反应生成盐和水进行分析.
解答 解:(1)用湿润的pH试纸测定盐酸的pH,再蘸取待测液滴在pH试纸上,稀释了待测溶液,使溶液的酸性减弱,当溶液的pH小于7时,呈酸性,且pH越小,酸性越强,则测得的pH结果比实际值偏大;
(2)紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝,盐酸显酸性,能使紫色石蕊溶液变红色;
(3)④为酸碱中和反应,可以是稀盐酸与氢氧化钠反应生成水和氯化钠,化学方程式为:HCl+NaOH=NaCl+H2O;
(4)⑤可能稀盐酸与铁锈反应生成盐和水,所以图中⑤的一种实际应用是:金属除锈.
故答案为:(1)偏大;
(2)紫色石蕊溶液变红色;
(3)HCl+NaOH=NaCl+H2O;
(4)金属除锈.
点评 本题主要考查了酸的性质的记忆,难度不大,需要在平时的学习中加强记忆即可完成.

练习册系列答案
相关题目
11.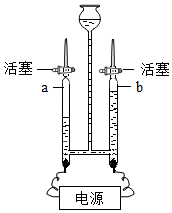 小明用如图装置进行水的电解实验,以下关于该实验说法错误的是( )
小明用如图装置进行水的电解实验,以下关于该实验说法错误的是( )
 小明用如图装置进行水的电解实验,以下关于该实验说法错误的是( )
小明用如图装置进行水的电解实验,以下关于该实验说法错误的是( )| A. | 在水中加入少量的氢氧化钠是为了增加导电性 | |
| B. | a管下方导线应接电源的负极 | |
| C. | a与b管内的气体质量比为2:1 | |
| D. | 可用带火星的木条来验证b管中的气体 |
18.欲除去下列物质中的少量杂质,所用试剂正确的是( )
| 物质 | 杂质 | 试剂 | |
| A | CO2 | SO2 | NaOH溶液 |
| B | KCl溶液 | K2SO4 | Ba(OH)2溶液 |
| C | CO2 | CO | Ca(OH)2溶液 |
| D | CaCO3 | CuSO4 | H2O |
| A. | A | B. | B | C. | C | D. | D |
15.下列化肥属于复合肥料的是( )
| A. | 碳酸氢铵 | B. | 氯化钾 | C. | 氨水 | D. | 磷酸二氢铵 |
13. 2017年4月13日消息,英国科技团队发明可食用水包,即利用液体塑成球形的技术,将水盛在双层薄膜中,下列有关水的说法中正确的是( )
2017年4月13日消息,英国科技团队发明可食用水包,即利用液体塑成球形的技术,将水盛在双层薄膜中,下列有关水的说法中正确的是( )
 2017年4月13日消息,英国科技团队发明可食用水包,即利用液体塑成球形的技术,将水盛在双层薄膜中,下列有关水的说法中正确的是( )
2017年4月13日消息,英国科技团队发明可食用水包,即利用液体塑成球形的技术,将水盛在双层薄膜中,下列有关水的说法中正确的是( )| A. | 水有自净能力,因此农药、化肥的大量使用不会造成水体污染 | |
| B. | 可食用水包中水分子不再运动 | |
| C. | 鉴别硬水和软水可用肥皂水 | |
| D. | 自然界中的水经过沉降、过滤、吸附后即可得到纯水 |
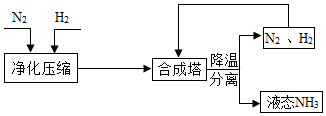 工业上合成 NH 3 的工艺流程可简化为:
工业上合成 NH 3 的工艺流程可简化为: 向含有CuSO4和HCl的混合溶液中逐滴加入一定量的NaOH溶液,充分反应,生成沉淀的质量(m1)与加入NaOH溶液的质量(m2)的关系如图所示,回答下列问题:
向含有CuSO4和HCl的混合溶液中逐滴加入一定量的NaOH溶液,充分反应,生成沉淀的质量(m1)与加入NaOH溶液的质量(m2)的关系如图所示,回答下列问题: