题目内容
5.下列图象正确反映所对应叙述关系的是( )
| A. | 向pH=3的溶液中不断加水 | |
| B. | 一定量的稀硫酸与锌粒反应 | |
| C. | 向MgCl2、CuSO4混合溶液中滴加NaOH | |
| D. | 煅烧一定质量的石灰石 |
分析 A、根据pH=3的溶液显酸性,溶液在稀释过程中,酸性减弱,pH值只会无限的接近7,但是永远不会等于或大于7进行分析;
B、根据锌和稀硫酸反应生成硫酸锌和氢气进行分析;
C、根据向稀硫酸和硫酸铜混合液中滴加氢氧化钠溶液,氢氧化钠会先与硫酸反应,再与硫酸铜反应,所以加入一定量的氢氧化钠后才会出现沉淀进行分析;
D、根据碳酸钙在高温的条件下生成氧化钙和二氧化碳进行分析.
解答 解:A、pH=3的溶液显酸性,溶液在稀释过程中,酸性减弱,pH值只会无限的接近7,但是永远不会等于或大于7,故A错误;
B、锌和稀硫酸反应生成硫酸锌和氢气,所以在锌粒中逐渐加入稀硫酸,氢气的质量从零开始逐渐增大,然后不变,故B错误;
C、向稀硫酸和硫酸铜混合液中滴加氢氧化钠溶液,氢氧化钠会先与硫酸反应,再与硫酸铜反应,所以加入一定量的氢氧化钠后才会出现沉淀,故C正确;
D、碳酸钙在高温的条件下生成氧化钙和二氧化碳,所以煅烧一定质量的石灰石,固体的质量最后不会减小到零,故D错误.
故选:C.
点评 本题是过程与图象结合题,是对学生识图能力的考查,解题的关键是能正确的分析各个反应的过程并能结合图象分析问题.

练习册系列答案
相关题目
15.某同学对Mg、Mn、Ag的金属活动性顺序进行探究.
提出假设:a.Mn的金属活动性比Mg强;b.Mn的金属活动性介于Mg和Ag之间
查阅资料:在相同条件下,金属与酸反应,产生气泡的速率越快,则该金属的活动性越强
实验设计:同温下,取大小相同的Mg、Mn、Ag三种金属薄片,分别投入等体积、等质量分数的足量稀盐酸中,观察现象.请回答:
(1)三种金属加入前都先用砂纸将表面擦光亮,其目的是③(填序号)
①使表面光亮,易观察现象 ②使反应金属温度相同,易反应 ③除去氧化膜,利于金属直接与酸反应
(2)根据表中的实验现象填空:
(3)结论:原假设中正确的是b(填“a”或“b”)
上述实验设计中,如果所用盐酸的溶质的质量分数不同,是否一定能得出正确的结论,并说明理由?不能,这是因为其它条件相同时,盐酸质量分数越大,反应速率越快.
提出假设:a.Mn的金属活动性比Mg强;b.Mn的金属活动性介于Mg和Ag之间
查阅资料:在相同条件下,金属与酸反应,产生气泡的速率越快,则该金属的活动性越强
实验设计:同温下,取大小相同的Mg、Mn、Ag三种金属薄片,分别投入等体积、等质量分数的足量稀盐酸中,观察现象.请回答:
(1)三种金属加入前都先用砂纸将表面擦光亮,其目的是③(填序号)
①使表面光亮,易观察现象 ②使反应金属温度相同,易反应 ③除去氧化膜,利于金属直接与酸反应
(2)根据表中的实验现象填空:
| / | Mn | Mg | Ag |
| 实验现象 | 产生气泡速率缓慢 | 产生气泡速率快 | 无任何现象 |
上述实验设计中,如果所用盐酸的溶质的质量分数不同,是否一定能得出正确的结论,并说明理由?不能,这是因为其它条件相同时,盐酸质量分数越大,反应速率越快.
13.下列物质,与Fe2O3、BaCl2、Na2CO3均能发生反应的是( )
| A. | 水 | B. | 澄清石灰水 | C. | 稀硫酸 | D. | 硫酸钠溶液 |
20.下列有关科学实验或现象的解释正确的是( )
| A. | 任何物质的饱和溶液,当温度降低时一定会析出溶质 | |
| B. | 揭开啤酒瓶盖,有大量的泡沫溢出说明气体的溶解度随温度的升高而减小 | |
| C. | 在研究氢氧化钠固体溶于水放热时,使用温度计的目的是搅拌以加快溶解 | |
| D. | 配制50g质量分数为10%的氯化钠溶液,用50mL量简量取所需水的体积 |
17.已知某物质在不同温度下的溶解度数据如表所示:
如果要配制该物质溶质质量分数为20%的饱和溶液400克,需要水320克,此时溶液的温度应为60℃.
| 温度(℃) | 0 | 20 | 40 | 60 | 80 |
| 溶解度(克) | 12.6 | 15.3 | 20.0 | 25.0 | 25.0 |
14.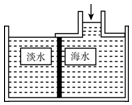 海水淡化可采用膜分离技术.如右图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入淡水池,而海水中的各种溶质不能通过淡化膜,从而得到淡水.对加压后右侧海水成分进行分析,错误的是( )
海水淡化可采用膜分离技术.如右图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入淡水池,而海水中的各种溶质不能通过淡化膜,从而得到淡水.对加压后右侧海水成分进行分析,错误的是( )
 海水淡化可采用膜分离技术.如右图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入淡水池,而海水中的各种溶质不能通过淡化膜,从而得到淡水.对加压后右侧海水成分进行分析,错误的是( )
海水淡化可采用膜分离技术.如右图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入淡水池,而海水中的各种溶质不能通过淡化膜,从而得到淡水.对加压后右侧海水成分进行分析,错误的是( )| A. | 海水的溶质质量分数不变 | B. | 溶剂质量减少 | ||
| C. | 海水质量减少 | D. | 溶质质量不变 |