题目内容
8.如图1是钠元素和氯元素在元素周期表中的信息和3种粒子的结构示意图.请回答下列问题: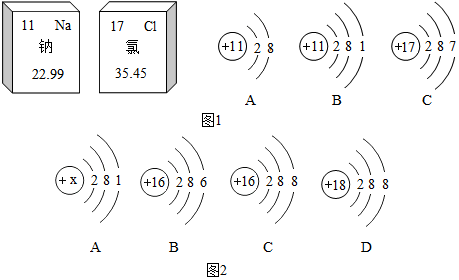
(1)氯原子的核电荷数是17;原子序数为11的原子的相对原子质量为22.99.
(2)钠原子与氯原子的最本质区别是核电荷数(或质子数)不同.
(3)在钠和氯气的反应中,得到电子的是氯原子;Na+的结构示意图是A(填标号).
(4)根据A、B、C、D四种粒子的结构示意图(如图2所示),回答问题:
①原子A中的X=11;
②以上四种粒子结构示意图中,表示稀有元素的粒子是D(填字母序号,下同),C和B属于同种元素的粒子.
分析 (1)根据元素周期表的信息来分析;
(2)根据不同种元素最本质的区别是质子数不同解答本题;
(3)根据原子结构以及离子结构示意图的画法来分析;
(4)原子中,质子数=核外电子数,根据元素的分类来分析.
解答 解:(1)由元素周期表的信息可知,氯原子的核电荷数是17;原子序数为11的钠原子的相对原子质量为22.99;故填:17;22.99;
(2)不同元素间最本质的区别是质子数不同,所以钠原子与氯原子的最本质区别是:核电荷数(或质子数)不同;故填:核电荷数(或质子数)不同;
(3)氯原子的最外层有7个电子,在化学反应中易得到一个电子;钠离子易失去一个电子而形成带一个单位正电荷的钠离子;故填:氯;A;
(4)①在原子中,质子数=核外电子数,X=2+8+1=11;故填:11;
②D是氩元素,属于稀有气体元素,BC的核电荷数相同,属于同种元素;故填:D;B.
点评 本题通过给出微粒的模型考查了学生的观察能力和对基本概念的理解与运用能力;了解元素周期表的特点及其应用,以及核外电子在化学反应中的作用是解题的关键.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
16. 如图为某一加碘食盐包装袋上的部分文字,下列说法错误的是( )
如图为某一加碘食盐包装袋上的部分文字,下列说法错误的是( )
 如图为某一加碘食盐包装袋上的部分文字,下列说法错误的是( )
如图为某一加碘食盐包装袋上的部分文字,下列说法错误的是( )| A. | 此食盐为混合物 | B. | KIO3是氧化物 | ||
| C. | 碘酸钾(KIO3)受热不稳定 | D. | KIO3中碘元素的化合价为+5价 |
18.实验室用燃烧法测定空气中氧气的含量,最适宜选用的物质是( )
| A. | 木炭 | B. | 红磷 | C. | 硫磺 | D. | 铁丝 |

