题目内容
11.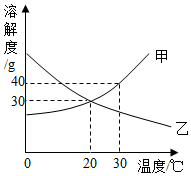 如图所示是甲、乙两种固体物质的溶解度曲线,请回答下列问题:
如图所示是甲、乙两种固体物质的溶解度曲线,请回答下列问题:(1)30℃时,把70g甲物质放入200g水中,降温到20℃出10g物质甲.
(2)若将20℃时130g乙的饱和溶液溶质质量分数减少到原来的一半,需加水的质量为130g.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)20℃时,甲物质的溶解度是30g,所以30℃时,把70g甲物质放人200g水中,降温到20℃出10g物质甲;
(2)20℃时乙物质的溶解度是30g,所以若将20℃时130g乙的饱和溶液溶质质量分数减少到原来的一半,需加水的质量为$\frac{30g}{\frac{30g}{130g}×100%×\frac{1}{2}}$-130g=130g.
故答案为:(1)10;
(2)130.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.2016年世界气象日的主题是“直面更热、更早、更涝的未来”,气候变化正在影响我们的自然环境和人类环境.下列有关环境问题的叙述正确的是( )
| A. | 为解决“白色污染”问题,可将废弃塑料焚烧处理 | |
| B. | 用二氧化碳和水等合成新型燃油,有利于减缓温室效应 | |
| C. | 为治理雾霾,禁止使用化石燃料 | |
| D. | 化工厂通过加高烟囱来排放废气,以防止形成酸雨 |
2. 小明同学为了测定市面销售的某品牌纯碱(杂质为氯化钠)中碳酸钠的质量分数,进行了如下实验:
小明同学为了测定市面销售的某品牌纯碱(杂质为氯化钠)中碳酸钠的质量分数,进行了如下实验:
①在三个烧杯中分别加入11.0g样品;
②向三个烧杯中分别加入一定质量的10.0%氯化钙溶液;
③将充分反应后生成的沉淀过滤、洗涤、干燥,并称量得到的白色固体.
实验所得数据见下表,请你分析并进行有关计算:
(1)样品中碳酸钠的质量是多少?
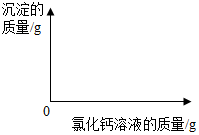
(2)在图中绘制出白色沉淀与加入氯化钙溶液的质量关系图(图上要注明白色沉淀、氯化钙溶液的相关质量).
(3)充分反应后,烧杯Ⅱ中氯化钠的溶质质量分数是多少?
 小明同学为了测定市面销售的某品牌纯碱(杂质为氯化钠)中碳酸钠的质量分数,进行了如下实验:
小明同学为了测定市面销售的某品牌纯碱(杂质为氯化钠)中碳酸钠的质量分数,进行了如下实验:①在三个烧杯中分别加入11.0g样品;
②向三个烧杯中分别加入一定质量的10.0%氯化钙溶液;
③将充分反应后生成的沉淀过滤、洗涤、干燥,并称量得到的白色固体.
实验所得数据见下表,请你分析并进行有关计算:
| 烧杯Ⅰ | 烧杯Ⅱ | 烧杯Ⅲ | |
| 加入10.0%氯化钙溶液的质量(g) | 55.5 | 120.0 | 150.0 |
| 白色固体的质量(g) | 5.0 | 10.0 | 10.0 |
(2)在图中绘制出白色沉淀与加入氯化钙溶液的质量关系图(图上要注明白色沉淀、氯化钙溶液的相关质量).
(3)充分反应后,烧杯Ⅱ中氯化钠的溶质质量分数是多少?
6.化学变化中可能伴随一些现象.对下列化学变化的现象描述正确的是( )
| A. | 红磷在空气中燃烧冒出大量白色烟雾 | |
| B. | 生石灰放入盛水的烧杯中,感到烧杯外壁发烫 | |
| C. | 铜放入稀盐酸中观察到大量气泡 | |
| D. | 铁丝在纯氧中燃烧生成黑色的四氧化三铁 |
16.“超临界水”因具有许多优良特质而被科学家追捧,它是指当气压和温度达到一定值时,水的液态和气态完全交融在一起的流体.下面有关“超临界水”的说法正确的是( )
| A. | 它是混合物 | |
| B. | 它是一种不同于水的物质 | |
| C. | 它的分子之间有间隔 | |
| D. | 它的一个分子由4个氢原子核2个氧原子构成 |
1.李铭同学想要探究甲、乙、丙三种物质溶解度的大小,于是他取来等质量的甲、乙、丙三种物质,并将它们分别放入三杯温度为t1℃的等质量的水中,用玻璃棒搅拌直至充分溶解,记录此时甲、乙、丙三种物质的剩余量情况,再将温度升温至t2℃,并再次记录下此时三种物质的剩余量情况,实验结束后李铭将记录的数据做成如表所示,下列说法中正确的是( )
| 物质 | 甲 | 乙 | 丙 |
| t1℃剩余质量(g) | 0 | 2 | 0.5 |
| t2℃剩余质量(g) | 2 | 0 | 3 |
| A. | t1℃时,甲物质的溶液一定是饱和溶液 | |
| B. | 甲物质的溶解度随温度的升高而增大 | |
| C. | t1℃和t2℃时,丙物质的溶液都为饱和溶液 | |
| D. | 乙物质的溶解度大于丙物质的溶解度 |

 2015年化学实验操作考试中,有同学在做铁与硫酸铜溶液反应实验时,意外发现铁丝的表面有少量无色无味的气体产生,事后他们对该现象产生浓厚兴趣,想探究该气体的成分.
2015年化学实验操作考试中,有同学在做铁与硫酸铜溶液反应实验时,意外发现铁丝的表面有少量无色无味的气体产生,事后他们对该现象产生浓厚兴趣,想探究该气体的成分. 如图是以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同,结合此图回答下列问题:
如图是以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同,结合此图回答下列问题: