题目内容
检验某溶液是否呈酸性,有四位同学分别设计下列4种方法,其中不正确的是( )
| A、在原溶液中滴加碳酸钠溶液,看是否有气泡产生 |
| B、在原溶液中滴加酚酞试液,看是否变色 |
| C、在原溶液中滴加紫色石蕊试液,看是否变色 |
| D、在原溶液中加入锌粒,看是否产生气泡 |
考点:酸的化学性质
专题:常见的酸 酸的通性
分析:根据酸的化学性质解答,酸性溶液能使紫色石蕊试液变红,能与 活泼金属反应产生氢气,能与碳酸钠溶液产生二氧化碳.
解答:解:A、酸性溶液能够和碳酸钠反应此时二氧化碳气体,可以检验溶液显酸性;
B、酸性和中性溶液中滴入酚酞试液都不变色,因此不能检验溶液显酸性;
C、石蕊试液变成红色,说明溶液显酸性,因此可以检验溶液显酸性;
D、锌能够和酸反应产生氢气,因此可以检验溶液显酸性;
故选B.
B、酸性和中性溶液中滴入酚酞试液都不变色,因此不能检验溶液显酸性;
C、石蕊试液变成红色,说明溶液显酸性,因此可以检验溶液显酸性;
D、锌能够和酸反应产生氢气,因此可以检验溶液显酸性;
故选B.
点评:本题考查了酸的化学性质,熟练掌握酸的化学性质及反应现象是解答本题关键,注意酚酞试液不变色,溶液可能显酸性,也可能显中性.

练习册系列答案
相关题目
下列实验操作中有错误的是( )
A、 硫在氧气里燃烧 |
B、 木炭在氧气里燃烧 |
C、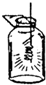 铁丝在氧气里燃烧 |
D、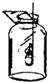 蜡烛在氧气里燃烧 |
把12克碳和48克氧气放在一个密封的容器中充分燃烧后,容器中的气体是( )
| A、一氧化碳 |
| B、二氧化碳 |
| C、一氧化碳和二氧化碳 |
| D、二氧化碳和氧气 |
下图中“○”和“●”分别表示两种不同的原子,其中能表示单质的是( )
A、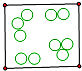 |
B、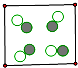 |
C、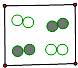 |
D、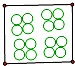 |
检验含CO32-的化合物,常使用的试剂是( )
| A、硫酸 |
| B、稀盐酸和澄清石灰水 |
| C、紫色石蕊试液 |
| D、澄清石灰水 |
在一密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下存在某个反应,测得反应前后各物质的质量如表
对该反应,下列描述正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 20 | 2 | 20 | 20 |
| 反应后质量/g | 2 | 待测 | 32 | 26 |
| A、该反应中甲、丙、丁的质量比为3:2:1 |
| B、乙在该反应中一定是催化剂 |
| C、待测质量一定为4 g |
| D、该反应是化合反应 |