题目内容
12.工业上常用煅烧石灰石的方法制取二氧化碳,现用含碳酸钙80%的石灰石生产880吨的二氧化碳,试计算需要石灰石的质量为多少?(CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑)分析 根据反应的化学方程式和提供的数据可以计算相关方面的问题.
解答 解:设需要石灰石的质量为x,
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,
100 44
x×80% 880t
$\frac{100}{x×80%}$=$\frac{44}{880t}$,
x=2500t,
答:需要石灰石的质量是2500t.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
2.一定发生化学变化的是( )
| A. | 冰雪融化 | B. | 矿石粉碎 | C. | 榨取果汁 | D. | 煤炭燃烧 |
20.下列实验现象描述不正确的是( )
| A. | 铁在氧气中燃烧生成四氧化三铁 | B. | 磷在氧气中燃烧产生大量的白烟 | ||
| C. | 硫在氧气中燃烧产生蓝紫色火焰 | D. | 镁条在氧气中燃烧生成白色固体 |
17.水是宝贵的自然资源,下列关于水的叙述正确的是( )
| A. | 淡水资源取之不尽,用之不竭 | |
| B. | 水由氢气和氧气组成 | |
| C. | 肥皂水不能区别开硬水和软水 | |
| D. | 为节约用水,改大水浸灌为喷灌、滴灌浇灌园林 |
1.某班级在实验室制取二氧化碳,老师观察到四个同学的如下操作,其中正确的是( )
| A. |  连接仪器 | B. | 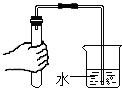 检查气密性 | C. |  取用石灰石 | D. |  验满 |
 铜锈成分的确定
铜锈成分的确定