题目内容
11.已知A、B、C、D、E是初中化学中常见的五种物质,其中A、B、C、D都含同一种元素,D、E是黑色粉末,A与D在高温条件下反应生成B,B和E可反应生成红色金属和A,将A通入澄清石灰水得到白色沉淀C,C与稀盐酸反应可得A,请推断回答:(1)写出下列物质的化学式:CCaCO3;ECuO.
(2)写出A与D反应的化学方程式CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
分析 根据题意,A、B、C、D、E是初中化学中常见的五种物质,其中A、B、C、D都含同一种元素,D、E是黑色粉末,A与D在高温条件下反应生成B,B和E可反应生成红色金属和A,将A通入澄清石灰水得到白色沉淀C,则生成的红色金属是铜,则E为氧化铜;二氧化碳能使澄清的石灰水变浑浊,A为二氧化碳,C为生成的碳酸钙;C与稀盐酸反应可得A,碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳;二氧化碳与碳在高温下反应生成一氧化碳,一氧化碳与氧化铜反应生成铜和二氧化碳,则B为一氧化碳,D为碳;据此进行分析解答.
解答 解:A、B、C、D、E是初中化学中常见的五种物质,其中A、B、C、D都含同一种元素,D、E是黑色粉末,A与D在高温条件下反应生成B,B和E可反应生成红色金属和A,将A通入澄清石灰水得到白色沉淀C,则生成的红色金属是铜,则E为氧化铜;二氧化碳能使澄清的石灰水变浑浊,A为二氧化碳,C为生成的碳酸钙;C与稀盐酸反应可得A,碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳;二氧化碳与碳在高温下反应生成一氧化碳,一氧化碳与氧化铜反应生成铜和二氧化碳,则B为一氧化碳,D为碳.
(1)C为碳酸钙,其化学式为CaCO3;E为氧化铜,其化学式为CuO.
(2)A与D反应,即二氧化碳与碳在高温下反应生成一氧化碳,反应的化学方程式为:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
故答案为:(1)CaCO3;CuO;(2)CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

练习册系列答案
相关题目
15.对宏观事实的微观解释错误的是( )
| A. | 温度升高,水银柱上升,是因为汞原子变大了 | |
| B. | 缉毒犬能发现毒贩,是因为分子是不断运动的 | |
| C. | 稀有气体能做保护气,是因为构成稀有气体的原子最外层达到稳定结构 | |
| D. | 稀盐酸和稀硫酸具有相似的化学性质是因为他们解离出的阳离子都是H+ |
16.下列实验操作正确的是( )
| A. | 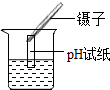 测定溶液的pH | B. | 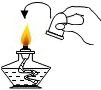 熄灭酒精灯 | C. | 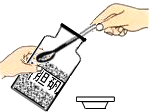 取用固体药品 | D. | 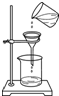 过滤操作 |
6.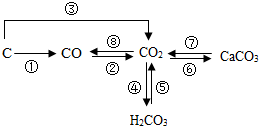 如图是部分含碳物质的转化关系图,根据图示判断下列说法正确的是( )
如图是部分含碳物质的转化关系图,根据图示判断下列说法正确的是( )
 如图是部分含碳物质的转化关系图,根据图示判断下列说法正确的是( )
如图是部分含碳物质的转化关系图,根据图示判断下列说法正确的是( )| A. | ①②③⑧都只能通过化合反应实现 | |
| B. | ⑤⑦均可用于实验室制取CO2 | |
| C. | 将CO2通入紫色石蕊溶液中,溶液变红,可用④来解释原因 | |
| D. | 图中物质均为含碳元素的化合物 |
3.下列图象能正确反映对应变化的是实验室中用一氧化碳还原氧化铁( )
| A. | 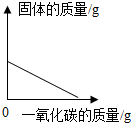 实验室用一氧化碳还原氧化铁 | |
| B. | 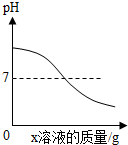 往氢氧化钙溶液中逐滴加入蒸馏水 | |
| C. |  向盐酸和氯化钙的混合溶液中逐滴加入碳酸钾溶液 | |
| D. | 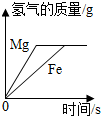 将足量粉末状金属分别与等质量、等质量分数的稀盐酸反应 |
1. 实验室中有一瓶标签受损的无色液体,如图所示,该液体只能是过氧化氢溶液和稀硫酸中的一种.可用的实验药品:二氧化锰、氯化钡溶液;仪器:试管,若需要其他仪器可自选.请用实验验证这瓶无色液体是什么?
实验室中有一瓶标签受损的无色液体,如图所示,该液体只能是过氧化氢溶液和稀硫酸中的一种.可用的实验药品:二氧化锰、氯化钡溶液;仪器:试管,若需要其他仪器可自选.请用实验验证这瓶无色液体是什么?
(1)这瓶无色液体不可能是蒸馏水,理由是由标签知该液体是混合物,而蒸馏水为纯净物.
(2)为验证该液体是什么,进行了如表实验:
(3)如果该液体是过氧化氢溶液,则上表步骤一中发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
 实验室中有一瓶标签受损的无色液体,如图所示,该液体只能是过氧化氢溶液和稀硫酸中的一种.可用的实验药品:二氧化锰、氯化钡溶液;仪器:试管,若需要其他仪器可自选.请用实验验证这瓶无色液体是什么?
实验室中有一瓶标签受损的无色液体,如图所示,该液体只能是过氧化氢溶液和稀硫酸中的一种.可用的实验药品:二氧化锰、氯化钡溶液;仪器:试管,若需要其他仪器可自选.请用实验验证这瓶无色液体是什么?(1)这瓶无色液体不可能是蒸馏水,理由是由标签知该液体是混合物,而蒸馏水为纯净物.
(2)为验证该液体是什么,进行了如表实验:
| 实验操作 | 实验现象 | 实验结论 |
| 步骤一:取该液体适量于试管中,向其中加入少量二氧化锰粉末. | 该液体不是 过氧化氢溶液. | |
| 步骤二:另取该液体适量于试管中,用胶头滴管(或滴管)向其中加入少量氯化钡溶液. | 产生白色沉淀 | 该液体是 稀硫酸. |
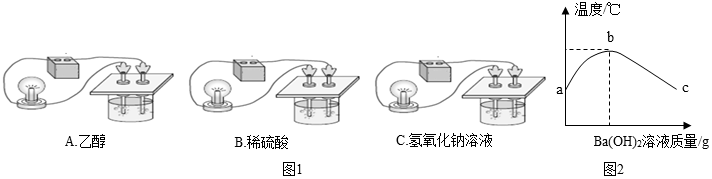
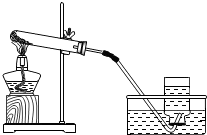 如图是实验室加热KClO3与MnO2的混合物制取氧气的装置图.
如图是实验室加热KClO3与MnO2的混合物制取氧气的装置图.