题目内容
4.现有一杯8%的氢氧化钠溶液50g,丹丹同学向烧杯中倒入50g稀硫酸后,用玻璃棒搅拌并测得完全反应后的溶液呈中性.2NaOH+H2SO4═Na2SO4+2H2O.(1)反应后溶液的pH=7(选填“>”“=”“<”).
(2)稀硫酸中溶质的质量分数是9.8%.
(3)计算上述反应后的溶液中溶质的质量分数.
分析 (1)溶液的酸碱性与溶液酸碱度的关系:pH>7,溶液呈碱性;pH=7,溶液呈中性;pH<7,溶液呈酸性;
(2)根据反应的化学方程式,由氢氧化钠的质量计算生成硫酸的质量;
(3)反应后的溶液中溶质的质量分数=$\frac{硫酸钠的质量}{反应后溶液的质量}$,根据反应的化学方程式,由氢氧化钠的质量计算生成硫酸钠的质量;利用质量守恒定律求反应后所得溶液的质量.
解答 解:(1)根据测得完全反应后的溶液呈中性,可判断,反应后溶液pH=7;故答案为:=;
(2)设硫酸的质量为x.
2NaOH+H2SO4=Na2SO4+2H2O
80 98
50g×8% x
则$\frac{80}{50g×8%}=\frac{98}{x}$,解得x=4.9g;
稀硫酸中溶质的质量分数是$\frac{4.9g}{50g}×100%$=9.8%.
(3)设反应后生成的硫酸钠质量为x.
2NaOH+H2SO4=Na2SO4+2H2O
80 142
50g×8% y
则$\frac{80}{50g×8%}=\frac{142}{y}$,解得y=7.1g
则反应后溶液中溶质的质量分数=$\frac{7.1g}{50g+50g}$×100%=7.1%
答:反应后的溶液中溶质的质量分数为7.1%.
点评 氢氧化钠溶液与稀硫酸完全后溶液呈中性,可判断两溶液恰好完全反应,反应既无气体也无沉淀,根据质量守恒定律,反应后所得溶液的质量=氢氧化钠溶液质量+稀硫酸的质量.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
19.阅读有关消毒剂的资料并回答相关问题:
(1)“84消毒液”是由次氯酸钠和表面活性剂混合配制的消毒剂,是一种无色或淡黄色液体,广泛用于公共场所和家庭卫生消毒,由于“84消毒液”有一定腐蚀性,将其稀释成0.2%~0.5%,浸泡时间为10到30分钟.
①次氯酸钠化学式为NaClO,其中氯元素的化合价为+1;
②使用“84消毒液”清洗衣服后要漂洗干净,其原因是84消毒液有腐蚀性.
(2)阅读下表,回答其它消毒剂相关问题:
对生活中不慎产生的外伤伤口进行消毒时,选用的合适消毒剂是H2O2,原因是双氧水具有较强的消毒杀菌能力,对人体没有腐蚀性.
(3)水是生命之源.为了保障我市居民饮用水的安全,自来水必需进行消毒处理.
①自来水厂处理水的过程中一般可先加入明矾,吸附水中悬浮的颗粒而沉降;
②在一些偏远农村一般用漂白粉作为水源消毒剂,漂白粉的有效成分为次氯酸钙,化学式是Ca(ClO)2.次氯酸钙很不稳定,能和空气中的某些成分反应生成CaCO3和次氯酸(HClO),后者见光分解生成盐酸并放出氧气,因而具有消毒杀菌作用.请写出次氯酸分解反应的化学方程式2HClO$\frac{\underline{\;光\;}}{\;}$2HCl+O2↑.
(4)ClO2是新一代饮用水的消毒剂,我国许多自来水厂采用ClO2代替Cl2来进行自来水消毒.请回答下列有关问题:
①ClO2读作二氧化氯,它属于氧化物(选填“单质”、“氧化物”或“混合物”).
②我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示:
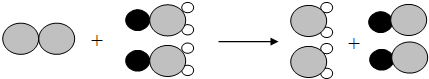
(其中“ ”表示氯原子,“
”表示氯原子,“ ”表示钠原子,“
”表示钠原子,“ ”表示氧原子)该反应的化学方程式为Cl2+2NaClO2=2NaCl+2ClO2.
”表示氧原子)该反应的化学方程式为Cl2+2NaClO2=2NaCl+2ClO2.
③由微观示意图得出的结论:化学反应前后原子的种类和个数不变.
(1)“84消毒液”是由次氯酸钠和表面活性剂混合配制的消毒剂,是一种无色或淡黄色液体,广泛用于公共场所和家庭卫生消毒,由于“84消毒液”有一定腐蚀性,将其稀释成0.2%~0.5%,浸泡时间为10到30分钟.
①次氯酸钠化学式为NaClO,其中氯元素的化合价为+1;
②使用“84消毒液”清洗衣服后要漂洗干净,其原因是84消毒液有腐蚀性.
(2)阅读下表,回答其它消毒剂相关问题:
| 消毒剂 | 化学式 | 性质和用途 | 注意事项 |
| 过氧乙酸溶液 | CH3COOOH | 过氧乙酸易挥发、易分解,其分解产物为醋酸和氧气.过氧乙酸具有很强的消毒杀菌能力,可以迅速杀灭各种微生物,包括病菌、细菌等 | 对皮肤有 腐蚀作用 |
| 双氧水 | H2O2 | 过氧化氢溶液俗称为双氧水,是一种无色液体,容易分解,其分解产物为水和氧气.双氧水具有较强的消毒杀菌能力. | 需低温 避光保存 |
(3)水是生命之源.为了保障我市居民饮用水的安全,自来水必需进行消毒处理.
①自来水厂处理水的过程中一般可先加入明矾,吸附水中悬浮的颗粒而沉降;
②在一些偏远农村一般用漂白粉作为水源消毒剂,漂白粉的有效成分为次氯酸钙,化学式是Ca(ClO)2.次氯酸钙很不稳定,能和空气中的某些成分反应生成CaCO3和次氯酸(HClO),后者见光分解生成盐酸并放出氧气,因而具有消毒杀菌作用.请写出次氯酸分解反应的化学方程式2HClO$\frac{\underline{\;光\;}}{\;}$2HCl+O2↑.
(4)ClO2是新一代饮用水的消毒剂,我国许多自来水厂采用ClO2代替Cl2来进行自来水消毒.请回答下列有关问题:
①ClO2读作二氧化氯,它属于氧化物(选填“单质”、“氧化物”或“混合物”).
②我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示:

(其中“
 ”表示氯原子,“
”表示氯原子,“ ”表示钠原子,“
”表示钠原子,“ ”表示氧原子)该反应的化学方程式为Cl2+2NaClO2=2NaCl+2ClO2.
”表示氧原子)该反应的化学方程式为Cl2+2NaClO2=2NaCl+2ClO2.③由微观示意图得出的结论:化学反应前后原子的种类和个数不变.
16.若用加热氯酸钾的方法制取氧气,忘记了加入二氧化锰,其结果会( )
| A. | 不产生氧气 | B. | 产生氧气,但反应速率较慢 | ||
| C. | 产生的氧气不纯 | D. | 氧气的产量减少,且反应速率较慢 |
13.下列说法正确的是( )
| A. | 地壳中含量最多的元素是硅 | |
| B. | 人体中含有多种元素,他们的多少直接影响着人体健康 | |
| C. | 最外层电子数决定元素的种类 | |
| D. | 高锰酸钾中含有两种元素 |
 A-G是初中科学常见物质.其中,A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀.如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.
A-G是初中科学常见物质.其中,A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀.如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.