题目内容
将含杂质的铁粉(杂质不与酸反应,不溶于水)10g加入50g稀硫酸中,恰好完全反应,过滤后,所得滤液质量为55.4g.则样品中杂质的质量分数是( )A.28%
B.56%
C.44%
D.缺少数据,无法确定
【答案】分析:随着铁与硫酸的反应,溶液的质量逐渐增加,根据反应的化学方程式,判断出溶液增加量与参加革命反应铁的质量关系,即可由反应前后溶液的增加求出样品中含铁的质量,从而求得样品中杂质的质量分数.
解答:解:设参加反应铁的质量为x
Fe+H2SO4═FeSO4+H2↑ 溶液质量增加
56 2 56-2=54
x 55.4g-50g=5.4g
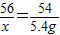
x=5.6g
则样品中杂质的质量分数=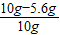 ×100%=44%
×100%=44%
故选C.
点评:根据题意判断随反应发生溶液质量会增加,此为解决问题的技巧,利用这一特殊关系,可使计算过程大为简化.
解答:解:设参加反应铁的质量为x
Fe+H2SO4═FeSO4+H2↑ 溶液质量增加
56 2 56-2=54
x 55.4g-50g=5.4g
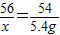
x=5.6g
则样品中杂质的质量分数=
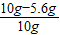 ×100%=44%
×100%=44%故选C.
点评:根据题意判断随反应发生溶液质量会增加,此为解决问题的技巧,利用这一特殊关系,可使计算过程大为简化.

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目