题目内容
9.我们学习了氧气的实验室制法,知道了制取气体的一般思路和方法.(Ⅰ)实验室制取气体时,确定发生装置需要常考虑的两种因素是AC(填序号).
A.反应物的状态 B.气体的密度 C.反应的条件 D.气体的溶解性
(Ⅱ)请根据下列装置图完成以下各题.
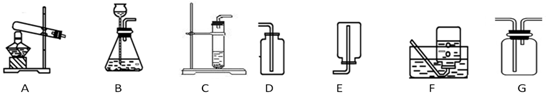
(1)以高锰酸钾为原料制取氧气,应选用A和D或F装置(填字母)来制取并
收集,反应的文字(或符号)表达式是高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气,或2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)若用F装置收集气体,需满足的条件是气体不能和水反应,不溶于水或不易溶于水_;
(3)A装置加热时,试管口略向下倾斜的原因是防止水蒸气冷凝、回流炸裂试管.
(Ⅲ)同学们想探究双氧水的浓度对反应速率的影响.在其他条件相同的情况下进行
了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
| 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 67 |
(2)写出上述反应的文字(或符号)表达式过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,或2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)实验3中,加入的二氧化锰质量为5g;
(4)相同条件下,实验3产生氧气的速率最快,说明反应与双氧水的浓度有关.
分析 (Ⅰ)根据制取气体的反应物状态、反应条件、气体的性质可以选择发生装置和收集装置;
(Ⅱ)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
为了防止高锰酸钾进入导管,通常在试管口塞一团棉花; 氧气的密度比空气的密度大,不易溶于水;
为了防止水蒸气冷凝、回流质量试管,深刻应该略向下倾斜;
(Ⅲ)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
根据实验现象可以判断相关方面的问题.
解答 解:(Ⅰ)实验室制取气体时,确定发生装置需要常考虑的两种因素是反应物的状态反应的条件.
故填:AC.
(Ⅱ)(1)以高锰酸钾为原料制取氧气需要加热,应该用A装置作为发生装置;
因为氧气的密度比空气大,可以用向上排空气法收集,即用D装置收集,氧气不易溶于水,可以用排水法收集,即用F装置收集;
反应的文字(或符号)表达式是:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气,或2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)若用F装置收集气体,需满足的条件是:气体不能和水反应,不溶于水或不易溶于水;
(3)A装置加热时,试管口略向下倾斜的原因是防止水蒸气冷凝、回流炸裂试管.
故填:A;D或F;高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气,或2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;气体不能和水反应,不溶于水或不易溶于水;防止水蒸气冷凝、回流炸裂试管.
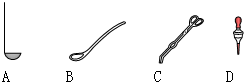
(Ⅲ)(1)取用二氧化锰的仪器是药匙B;
(2)过氧化氢分解生成水和氧气,反应的文字(或符号)表达式为:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,或2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)为了进行对比,实验3中,加入的二氧化锰质量为5g;
(4)相同条件下,实验3产生氧气的速率最快,说明反应与双氧水的浓度有关,即其它条件相同时,反应物浓度越大,反应速率越快.
故填:B;过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,或2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;5;浓度.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

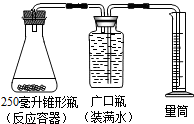 某同学采用如图装置,用一些植物的器官来代替MnO2作催化剂,分解H2O2制取氧气(2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑),记录数据如表.
某同学采用如图装置,用一些植物的器官来代替MnO2作催化剂,分解H2O2制取氧气(2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑),记录数据如表.| 序号 | H2O2溶液的 质量(克) | H2O2溶液的 溶质质量分数 | 植物的器官及质量 | 收集气体的体积(毫升) | 收集气体的时间(分钟) |
| 1 | 34 | 15% | 大颗粒胡萝卜16克 | 80 | 18 |
| 2 | 34 | 15% | 大颗粒马铃薯16克 | 80 | 10.5 |
| 3 | 34 | 15% | 小颗粒马铃薯16克 | 80 | 4 |
(1)要使胡萝卜能够更快地促进过氧化氢的分解,可采用的方法是将胡萝卜切成更小的颗粒.
(2)当量筒内的水达到250毫升时,打开广口瓶的 橡皮塞,立即将带火星的木条伸入瓶内,却发现木条不能复燃. 请你解释木条不能复燃的原因是:氧气的纯度不够高.
(3)34克15%的H2O2的质完全分解,能制得氧气2.4克.已知标准气压下氧气的密度是1.43克/升,则制得的氧气体积是1.678×10-3米3.
| A. | 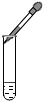 向试管中滴加液体 | B. | 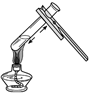 给试管中液体加热 | ||
| C. | 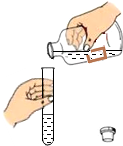 向试管中倾倒液体 | D. | 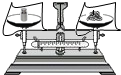 称取一定质量的食盐 |
| A. | 原子中一定含有质子、中子、电子 | |
| B. | 单质中只含有一种元素,因此只含有一种元素的物质一定是单质 | |
| C. | 稀有气体元素的原子最外层电子数为8(氦除外),因此微粒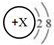 一定是稀有气体元素的原子 一定是稀有气体元素的原子 | |
| D. | 补铁酱油、高钙牛奶中的“铁”、“钙”指的是元素 |
 有A、B、C、D四种物质,如图所示,A、B、C在一定下可以发生转化,在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A.D与A、B、C均能发生反应,D与C发生中和反应,D与A反应时有CO2气体产生,但不能持续产生(反应物均没有消耗完).
有A、B、C、D四种物质,如图所示,A、B、C在一定下可以发生转化,在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A.D与A、B、C均能发生反应,D与C发生中和反应,D与A反应时有CO2气体产生,但不能持续产生(反应物均没有消耗完).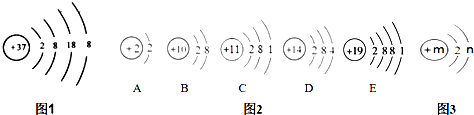
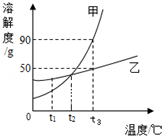 作图法是常用的数据处理方法,甲、乙两种物质的溶解度曲线如图所示,根据图示回答下列问题:
作图法是常用的数据处理方法,甲、乙两种物质的溶解度曲线如图所示,根据图示回答下列问题: