题目内容
12. 暖宝宝是一种使用便捷、安全的贴身发热品,如图所示,使用前撕开暖贴的真空包装袋,揭去后面的衬纸,贴在内衣的外侧,用手铺平即可,可贴于人体的肩部、背部、腰部、胃部及相关关节部位.小科同学对暖宝宝的发热原理产生了好奇并进行了科学探究.
暖宝宝是一种使用便捷、安全的贴身发热品,如图所示,使用前撕开暖贴的真空包装袋,揭去后面的衬纸,贴在内衣的外侧,用手铺平即可,可贴于人体的肩部、背部、腰部、胃部及相关关节部位.小科同学对暖宝宝的发热原理产生了好奇并进行了科学探究.【阅读说明书】暖宝宝的袋子有两层,外袋是不透气的明胶层,内层由无纺布组成,采用微孔透气膜制作的.在使用时,去掉外袋,让内袋(无纺布袋)贴在衣服上就可以缓慢放热.
【初步探究】小科剪开了内袋,发现里面装的是一些黑色粉末.
【提出猜想】该黑色粉末可能是碳粉、铁粉、二氧化碳、氧化铜、四氧化三铁中的一种或几种.
【初步验证】将磁铁靠近黑色粉末,部分被吸引.
【查阅资料】四氧化三铁具有磁性,能被铁吸引.
【得出结论】该黑色粉末可能含有的物质:铁粉或四氧化三铁或它们的混合物.
【设计实验】
| 实验操作 | 实验现象 | 解释或结论 | |
| 步骤1 | 取A、B两袋相同的“暖宝宝”,A袋打开外袋取出内袋;B袋不打开外袋,放置在同样的环境中 | A袋“暖宝宝”温度很快上升; AB袋温度没有明显变化 | “暖宝宝”发热是由于袋内物质与 氧气接触. |
| 步骤2 | 一天后,从上述A、B两袋中各取少量袋内物质于两支试管中,分别加入适量稀盐酸 | A袋内物质部分溶解,溶液呈黄色;B袋内物质部分溶解,产生气体,溶液变成浅绿色.(已知:FeCl3溶液呈黄色) | A袋内物质中的铁已经转化为氧化铁; B袋内该物质与稀盐酸反应的化学方程式为: Fe+2HCl=FeCl2+H2↑ |
分析 由题目给出的信息可知:将磁铁接近黑色粉末,部分被吸收,因此该黑色粉末可能含有铁粉或四氧化三铁或它们的混合物;铁在与氧气和水充分接触时容易发生化学反应,反应过程中放出热量,从而使得“暖宝宝”为人体提供热量.铁在只有水没有氧气存在的情况下不容易生锈.“暖宝宝”发出的热量主要来自铁粉发生氧化(生锈)的过程,该过程将化学能转化为热能.
解答 解:【得出结论】将磁铁接近黑色粉末,部分被吸收,因此该黑色粉末可能含有铁粉或四氧化三铁或它们的混合物,故答案为:铁粉或四氧化三铁或它们的混合物;
【设计实验】
暖宝宝发热是由于袋内物质与氧气接触的结果.故填:氧气.
B袋内的铁没有反应,当加入稀盐酸时铁能和稀盐酸反应生成氢气和氯化亚铁,氯化亚铁溶液是浅绿色的,方程式为Fe+2HCl=FeCl2+H2↑.故填:Fe+2HCl=FeCl2+H2↑.
【得出结论】“暖宝宝”发出的热量主要来自铁粉发生氧化(生锈)的过程,该过程将化学能转化为热能.
故填:化学.
点评 解答本题的关键是要掌握化学方程式的书写方法、铁生锈的条件、探究实验的设计方法等方面的知识,只有这样才能对问题做出正确的判断.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.如图甲所示是医院给病人输液用的一次性输液恒温器,化学兴趣小组的同学进行了一系列探究活动,请你一起参与他们的探究活动.
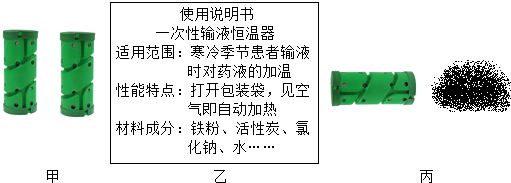
探究Ⅰ恒温器的发热原理是什么?
小组同学查阅“使用说明书”(如图乙所示),经讨论一致认为一次性输液恒温器主要是通过铁的锈蚀反应产生热量的.请写出铁锈蚀的条件铁与空气、水共存.
探究Ⅱ活性炭和氯化钠的作用是什么?
[猜想假设]活性炭、氯化钠均可加快铁的锈蚀,使其在短时间内放出较多热量.
[设计方案并实验]取一定质量的铁粉与水混合均匀,然后平均分成A、B、C、D四份,分别放入洁净的烧杯中,按如下方案在空气中进行实验,并记录实验现象.请填写表中空白:
[分析讨论]将实验A与B、实验A与C进行对比,得出活性炭和氯化钠均可加快铁的锈蚀;将实验D与实验A、B、C(填字母序号)进行对比,得出活性炭和氯化钠同时存在时铁的锈蚀速度更快.
探究Ⅲ使用后恒温器内物质的主要成分是什么?
[实物观察]使用后恒温器内的物质是黑褐色粉末(如图丙所示)
[查阅并分析]通过查阅资料,并根据恒温器的发热原理,大家认为黑褐色粉末中一定含有氧化铁、铁的氢氧化物(能与酸反应)和氯化钠.
[提出问题]使用后恒温器内的黑褐色粉末除氧化铁、铁的氢氧化物和氯化钠外,还有什么物质?
[假设猜想]猜想一:还含有铁粉;猜想二:还含有活性炭;猜想三:还含有活性炭和碳粉.
[设计方案并实验]取黑褐色粉末于洁净的试管中,加足量稀硫酸.观察到的现象有:
(1)有气泡产生,(2)黑色粉末部分溶解.证明猜想三正确.写出产生现象(1)的化学方程式Fe+H2SO4═FeSO4+H2↑.
[反思拓展]一次性输液恒温器利用铁的缓慢氧化为人类提供了热量,由此可见,人们在生产和生活中可以利用化学反应放出的能量,请再举一例做饭(或炼铁等,合理即可).

探究Ⅰ恒温器的发热原理是什么?
小组同学查阅“使用说明书”(如图乙所示),经讨论一致认为一次性输液恒温器主要是通过铁的锈蚀反应产生热量的.请写出铁锈蚀的条件铁与空气、水共存.
探究Ⅱ活性炭和氯化钠的作用是什么?
[猜想假设]活性炭、氯化钠均可加快铁的锈蚀,使其在短时间内放出较多热量.
[设计方案并实验]取一定质量的铁粉与水混合均匀,然后平均分成A、B、C、D四份,分别放入洁净的烧杯中,按如下方案在空气中进行实验,并记录实验现象.请填写表中空白:
| A | B | C | D | |
| 实验方案 | 铁粉和水的混合物 | 在铁粉和水的混合物中加入ag活性炭,混匀后静置 | 在铁粉和水的混合物中加入ag氯化钠,混匀后静置 | 在铁粉和水的混合物中加入ag活性炭和ag氯化钠,混匀后静置 |
| 实验现象 | 铁粉较慢锈蚀 | 铁粉较快锈蚀 | 铁粉较快锈蚀 | 铁粉很快锈蚀 |
探究Ⅲ使用后恒温器内物质的主要成分是什么?
[实物观察]使用后恒温器内的物质是黑褐色粉末(如图丙所示)
[查阅并分析]通过查阅资料,并根据恒温器的发热原理,大家认为黑褐色粉末中一定含有氧化铁、铁的氢氧化物(能与酸反应)和氯化钠.
[提出问题]使用后恒温器内的黑褐色粉末除氧化铁、铁的氢氧化物和氯化钠外,还有什么物质?
[假设猜想]猜想一:还含有铁粉;猜想二:还含有活性炭;猜想三:还含有活性炭和碳粉.
[设计方案并实验]取黑褐色粉末于洁净的试管中,加足量稀硫酸.观察到的现象有:
(1)有气泡产生,(2)黑色粉末部分溶解.证明猜想三正确.写出产生现象(1)的化学方程式Fe+H2SO4═FeSO4+H2↑.
[反思拓展]一次性输液恒温器利用铁的缓慢氧化为人类提供了热量,由此可见,人们在生产和生活中可以利用化学反应放出的能量,请再举一例做饭(或炼铁等,合理即可).
3.如图所示:某两种物质在一定条件下能发生化学反应.则下列说法中正确的是( )
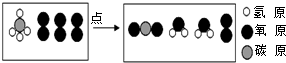

| A. | 该反应是氧化反应 | |
| B. | 该图示体现的是置换反应 | |
| C. | 反应前后分子和原子种类都不变 | |
| D. | 该反应中,参加反应的两种物质分子数之比是1:3 |
20.下列变化不属于化学变化的是( )
| A. | 牛奶变酸 | |
| B. | 将室温下的饱和澄清石灰水升高温度后变浑浊 | |
| C. | 用过氧化氢溶液制氧气 | |
| D. | 氢氧化钠溶液使酚酞变红 |
18.章章和卢卢都非常喜欢做科学探究实验,不仅能动脑筋思考,同时还锻炼了自己的动手能力提高了处理特殊情况的能力.下列有关他俩儿对实验设计的方案中,达不到实验目的是( )
| A. | 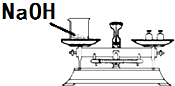 称取氢氧化钠固体 | |
| B. | 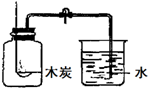 探究空气中氧气体积分数 | |
| C. | 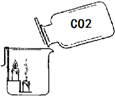 验证CO2 密度比空气大且不能燃烧也不支持燃烧 | |
| D. | 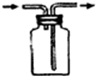 收集H2 |