题目内容
在天平两端的烧杯中,分别盛有100g溶质质量分数为7.3%的稀盐酸,调节天平平衡后,向左边烧杯中加入 2.2g Fe2O3,要使充分反应后天平仍然保持平衡,需向右边烧杯中加入金属镁的质量为
A.2.4 g B.2.2g C.3.2g D.3.6 g
A
【解析】
试题分析:氧化铁与盐酸反应生成的氯化铁和水,没有生成气体故左边烧杯中增加的质量为2.2g;要使充分反应后天平仍然保持平衡,那么右边的天平的质量也增加2.2g。镁与盐酸反应生成的是氯化镁和氢气,设加入金属镁的质量为x,那么生成的氢气的质量x-2.2g。
Mg +2 HCl == MgCl2 + H2 ↑
24 2
X x-2.2g
24/x =2/x-2.2g
X=2.4g ,故选A。
考点:有关化学方程式的计算

练习册系列答案
相关题目
(5分)某化学实验小组要检测黄铜(铜、锌合金)中金属铜的纯度,同学们取20g黄铜样品,向其中分三次共加入15g盐酸溶液,充分反应后测得实验结果如下:
实验次数 | 1 | 2 | 3 |
盐酸质量 | 5g | 5g | 5g |
氢气质量 | 0.04g | m | 0.02g |
请计算:(1)第二次实验产生氢气的质量m= g。
(2)黄铜(铜、锌合金)中金属铜的纯度。

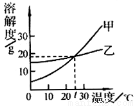
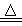 2R+4K2O+3O2↑,则R的化学式为 .
2R+4K2O+3O2↑,则R的化学式为 .