��Ŀ����
11��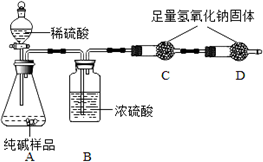 ijƷ�ƴ����к��������Ȼ��ƣ�ij��ѧ̽��С�����ⶨ��Ʒ�ƴ���Ĵ��ȣ���̼���Ƶ�������������
ijƷ�ƴ����к��������Ȼ��ƣ�ij��ѧ̽��С�����ⶨ��Ʒ�ƴ���Ĵ��ȣ���̼���Ƶ���������������һ������ͬѧ�����ͼ��ʾʵ�飺
��ʵ�鲽�衿
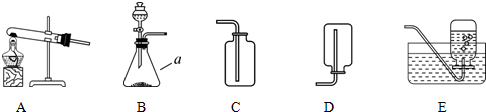
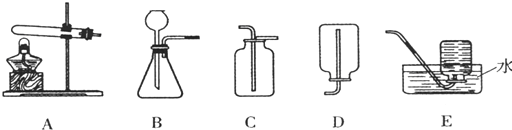
����װ����ͼ�����������װ�õ������ԣ�
�ڳ�ȡ13.0g��Ʒ������ƿ�У�������������ˮ�ܽ⣬��������װ���м�����Ӧ��ҩƷ��
�۳���װ��C��������
�ܴ�Һ©����������ϡ���ᣬֱ�����ٲ�������Ϊֹ��
���ٴγ���װ��C ����������
�������Ʒ��̼���Ƶ�����������
��ʵ�������
��1��Aװ���з�Ӧ�Ļ�ѧ����ʽΪNa2CO3+H2SO4=Na2SO4+H2O+CO2����
��2��Bװ�õ������dz�ȥˮ������
��3�����û��Bװ����������Ʒ��̼���Ƶ���������ƫ����ƫ��ƫС�����䣩
��4��С������ܷ�������������ͬѧ�Ǿ���������Ϊ���ܣ�����������ӷ����Ȼ������屻װ��C���գ�Ӱ��ʵ��ⶨ��
��5���Ƶô�����Ʒ������Ϊ13.0g��ʵ��ǰ����Cװ�ã�����ҩƷ���������ֱ�Ϊ61.2g��65.6g����ô�����Ʒ�Ĵ���Ϊ81.5%����ȷ��0.1%����
����������ͬѧ�������ɳ����ķ������ⶨ��Ʒ�д���������������������ͼʵ�飺
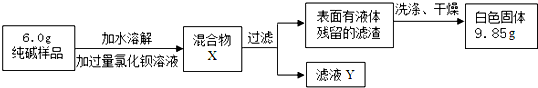
��1���жϼ����Ȼ�����Һ�Ƿ�����ĺ��ʷ�����A��Ȼ��۲������жϣ�
A�����û����X�����ϲ���Һ�м����μ��Ȼ�����Һ�����ް�ɫ�������ɣ����Ȼ����Ѿ�������
B��������X�еμ�ϡ���ᣬ���а�ɫ����������˵���Ȼ����Ѿ�������
��2���ж������Ƿ�ϴ�Ӹɾ������Բ�ȡ������ϴ��Һ�еμ�C��Ȼ��۲������жϣ�
A���Ȼ�����Һ B��ϡ���� C����������Һ D��ϡ����
��3������ʵ�����ݣ���������Ʒ��̼���Ƶ���������Ϊ88.3%����ȷ��0.1%����
��ʵ�鷴˼��
��������ͬѧ�����Ʒ����̼���Ƶ���������������Ϊ���飨��ס����ҡ�����ȷ����һ����ڽϴ�ƫ���ԭ�����������������ɵĶ�����̼��������ƿ�У�δ��װ��C���գ�Ӱ��ʵ��ⶨ��
���� ��ʵ�鲽�衿�ٸ���ʵ����ȡ��������Ҫװ�õ������Խ��н��
��ʵ���������1������̼���ƺ����ᷴӦ���������ơ�ˮ�Ͷ�����̼���н��
��2������Ũ���������ˮ�Խ��н��
��3������Cװ�������ӵ������������ɵĶ�����̼�����������û��Bװ�ã���ʹ������ɶ�����̼������������н��
��4����������ӷ����Ȼ������屻װ��C���գ�Ӱ��ʵ��ⶨ���н��
��5������Cװ��ǰ���������ӵ������������ɵĶ�����̼���������н��
��������1�������Ȼ�����Һ��̼���Ʒ�Ӧ����̼�ᱵ�������н��
��2�������Ȼ��ƺ���������Һ��Ӧ�����Ȼ�����ɫ�������н��
��3�����ݰ�ɫ����������ɵ�̼�ᱵ���������̼���Ƶ��������ɣ�
��ʵ�鷴˼����������������ɵĶ�����̼��������ƿ�У�δ��װ��C���գ�Ӱ��ʵ��ⶨ���н��
��� �⣺��ʵ�鲽�衿�ٸ���ʵ����ȡ��������Ҫװ�õ������ԣ�
��ʵ���������1��̼���ƺ����ᷴӦ���������ơ�ˮ�Ͷ�����̼��Aװ���з�Ӧ�Ļ�ѧ����ʽΪNa2CO3+H2SO4=Na2SO4+H2O+CO2����
��2��Ũ���������ˮ�ԣ�����Bװ�õ������dz�ȥˮ������
��3��Cװ�������ӵ������������ɵĶ�����̼�����������û��Bװ�ã���ʹ������ɶ�����̼��������������̼���Ƶ�����Ҳ���࣬��û��Bװ����������Ʒ��̼���Ƶ���������ƫ��
��4������ӷ����Ȼ������屻װ��C���գ�Ӱ��ʵ��ⶨ�����Բ���������������
��5������Ʒ��̼���Ƶ�����Ϊx��
������̼������=65.6g-61.2g=4.4g
Na2CO3+H2SO4=Na2SO4+H2O+CO2����
106 44
x 4.4g
$\frac{106}{44}=\frac{x}{4.4g}$
x=10.6g
��Ʒ��̼���Ƶ���������=$\frac{10.6g}{13.0g}��$100%=81.5%
����Ʒ��̼���Ƶ���������Ϊ81.5%��
��������1���Ȼ�����Һ��̼���Ʒ�Ӧ����̼�ᱵ�����������жϼ����Ȼ�����Һ�Ƿ�����ĺ��ʷ����Ǿ��û����X�����ϲ���Һ�м����μ��Ȼ�����Һ�����ް�ɫ�������ɣ����Ȼ����Ѿ�������
��2���Ȼ��ƺ���������Һ��Ӧ�����Ȼ�����ɫ�����������ж������Ƿ�ϴ�Ӹɾ������Բ�ȡ������ϴ��Һ�еμ���������Һ��
��3����ԭ�������̼���Ƶ�������y
Na2CO3+BaCl2=BaCO3��+2NaCl
106 197
y 9.85g
$\frac{106}{197}=\frac{y}{9.85g}$
y=5.3g
��������Ʒ��̼���Ƶ���������=$\frac{5.3g}{6.0g}��100%$=88.3%
����������Ʒ��̼���Ƶ���������Ϊ88.3%��
��ɫ����������ɵ�̼�ᱵ���������̼���Ƶ��������ɣ�
��ʵ�鷴˼����������������ɵĶ�����̼��������ƿ�У�δ��װ��C���գ�Ӱ��ʵ��ⶨ�����Լ�������ͬѧ�����Ʒ����̼���Ƶ����������������ȷ��
�ʴ�Ϊ��
��ʵ�鲽�衿��װ�õ������ԣ�
��ʵ���������1��Na2CO3+H2SO4=Na2SO4+H2O+CO2������2����ȥˮ��������3��ƫ��4������ӷ����Ȼ������屻װ��C���գ�Ӱ��ʵ��ⶨ����5��81.5��
��������1��A����2��C����3��88.3��
��ʵ�鷴˼���ң�����������ɵĶ�����̼��������ƿ�У�δ��װ��C���գ�Ӱ��ʵ��ⶨ��
���� ������һ��ʵ��̽���ۺ��⣬��ֵ�չʾ�˻�ѧ֪ʶ�ķ������棬�����ۺ���ǿ�ѶȽϴ�ѵ��ѧ�����õ�˼άƷ���Լ�֪ʶ���������нϺõİ�����

 Сѧ��ʱ��ҵȫͨ����ϵ�д�
Сѧ��ʱ��ҵȫͨ����ϵ�д� �����ÿ�ʱѵ��ϵ�д�
�����ÿ�ʱѵ��ϵ�д� ��Ԫȫ��������ϵ�д�
��Ԫȫ��������ϵ�д� �»ƸԱ����ܾ�ϵ�д�
�»ƸԱ����ܾ�ϵ�д�| A�� | ������ | B�� | ���ͻӷ� | C�� | �·�ɹ�� | D�� | �������� |
| A�� | �������� ���� NaOH | B�� | ����� ����ľ�� K2SO4 | ||
| C�� | ����ͭ���� ���� CuSO4•5H2O | D�� | �������� �� ��ʯ�� Ca��OH��2 |