题目内容
16.将A、B、C各10克混合均匀后加热,A全部参加反应生成3克D,同时增加9克C,则反应中A和B的质量比为( )| A. | 1:5 | B. | 1:4 | C. | 5:1 | D. | 4:1 |
分析 根据质量守恒定律定义:参加化学反应的各物质质量总和等于反应后生成的各物质质量总和.
解答 解:根据A完全参加了反应,说明A是反应物,并且参加反应的A质量为10g,生成了3 g D,说明D是生成物,同时增加了9 g C,说明C是生成物,并且生成了9g C,所以生成物是D和C质量和为12g,由于反应物如果只是A的话,质量才10g,所以B也应该是反应物,参加反应的质量为12g-10g=2g,所以反应中A和B的质量比为10g:2g=5:1.
故选C.
点评 通过回答本题要知道根据题给信息要会判断,谁是反应物,谁是生成物,质量增加就是生成物,质量减少就是反应物.

练习册系列答案
相关题目
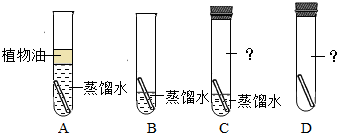
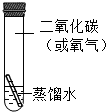
6.下列实验操作正确的是( )
| A. |  | B. | 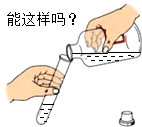 | C. | 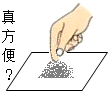 | D. | 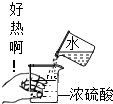 |
7.如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
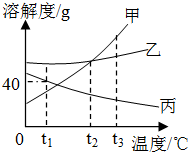

| A. | t2℃时,甲、乙两种物质的溶解度相等 | |
| B. | 当甲中含少量乙时,可用冷却热饱和溶液的方法提纯甲 | |
| C. | 分别将t3℃时等质量的甲、乙、丙的饱和溶液降温至t1℃,析出晶体最多的是甲 | |
| D. | t1℃时,某同学将40克丙固体加入60克水中,配成了溶质的质量分数为40%的丙溶液 |
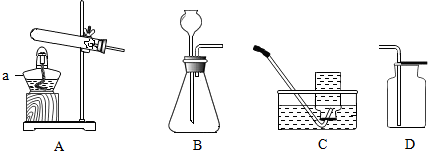
4.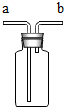 如图所示装置可用于气体的收集、检验、除杂和体积的测量,用如图不能完成的实验是( )
如图所示装置可用于气体的收集、检验、除杂和体积的测量,用如图不能完成的实验是( )
 如图所示装置可用于气体的收集、检验、除杂和体积的测量,用如图不能完成的实验是( )
如图所示装置可用于气体的收集、检验、除杂和体积的测量,用如图不能完成的实验是( )| A. | 气体从a端通入,收集O2 | |
| B. | 瓶内装有澄清石灰水,检验O2中是否含CO2 | |
| C. | 瓶内装有浓H2SO4溶液,吸收CO2中混有的水蒸气 | |
| D. | 在b端接量筒,瓶内装满水,测量气体的体积 |
11.下列关于实验的操作或方法,错误的是( )
| A. | 可燃性气体点燃之前必须检验气体的纯度 | |
| B. | 用胶头滴管向试管中滴加液体时,为防止液体外漏应将滴管伸入试管内滴加 | |
| C. | 用托盘天平称量固体药品时,药品应放在左盘,砝码放在右盘 | |
| D. | 稀释浓硫酸时,应将浓硫酸慢慢加到蒸馏水中并及时搅拌 |
1.要除去下列物质中的少量杂质括号内的物质为杂质,所选用试剂不正确的是( )
| A. | CO2 (O2):灼热的铜粉 | B. | CH4 (H2O):浓硫酸 | ||
| C. | CO (CO2):氢氧化钠溶液 | D. | NaOH (Na2CO3):盐酸 |
5.氢氧化钠固体易吸收空气中的二氧化碳而变质.取4.65g已经部分变质的氢氧化钠固体与36.5g10%的盐酸恰好完全反应后,将溶液蒸干,所得固体的质量为( )
| A. | 11.7g | B. | 1.17g | C. | 5.85g | D. | 58.5g |
 .
.