题目内容
8.有一氯化钠样品中混有少量硝酸钾(再无其他杂质),现进行如下实验:取样品5.0g,加水溶解,滴入10%的硝酸银溶液至85.0g时再无白色沉淀生成.(1)该反应的基本反应类型为复分解反应
(2)求样品中硝酸钾的质量分数.
分析 (1)根据氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠,根据反应类型解答;
(2)样品中硝酸钾的质量分数=$\frac{样品质量-氯化钠质量}{样品质量}$×100%,由消耗的硝酸银的质量,根据反应的化学方程式,计算出氯化钠的质量;
解答 解:
(1)氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠,是两种化合物相互交换成分生成另外两种化合物的反应,属于复分解反应;
(2)设恰好完全反应时,参加反应的氯化钠的质量为x,85.0g10%的硝酸银溶液中硝酸银的质量=85.0g×10%=8.5g
NaCl+AgNO3═AgCl↓+KNO3
58.5 170
x 8.5g
$\frac{58.5}{x}=\frac{170}{8.5g}$
x=2.925g
样品中硝酸钾的质量分数=$\frac{2.925g}{5g}×$100%=58.5%
答案:
(1)复分解反应
(2)样品中硝酸钾的质量分数是 58.5%
点评 根据质量守恒定律,反应后所得溶液的质量=样品质量+溶解所加水的质量+反应所加硝酸银溶液的质量-反应生成沉淀的质量.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.化学性质稳定且通电会发出不同颜色的光,常用于填充霓虹灯的气体是 ( )
| A. | 稀有气体 | B. | 氮气 | C. | 氧气 | D. | 二氧化碳 |
3.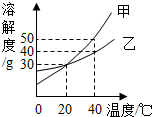 如图是甲、乙两种固体的溶解度曲线,下列说法正确的是( )
如图是甲、乙两种固体的溶解度曲线,下列说法正确的是( )
 如图是甲、乙两种固体的溶解度曲线,下列说法正确的是( )
如图是甲、乙两种固体的溶解度曲线,下列说法正确的是( )| A. | 甲的溶解度等于乙的溶解度 | |
| B. | 20℃时,100g乙的饱和溶液中溶质质量是30g | |
| C. | 降低温度,有可能将甲的不饱和溶液变为饱和溶液 | |
| D. | 40℃时,分别用100g水配制甲、乙的饱和溶液,所需乙的质量大于甲的质量 |
13.下列对于氢气在空气中燃烧的说法,错误的是( )
| A. | 氢气在空气中燃烧时,发出淡蓝色火焰 | |
| B. | 氢气燃烧时会放出大量的热 | |
| C. | 氢气燃烧时会产生浓烈的刺激性气味 | |
| D. | 氢气燃烧属于化合反应 |
20.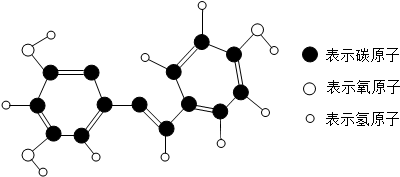 现代科技证明,白藜芦主要来源于葡萄、花生、桑椹等植物,红葡萄酒中含有的白藜芦醇具有抗氧化、抗癌和预防心血管疾病的作用,其分子模型如图所示,下列关于白藜芦醇的说法错误的是( )
现代科技证明,白藜芦主要来源于葡萄、花生、桑椹等植物,红葡萄酒中含有的白藜芦醇具有抗氧化、抗癌和预防心血管疾病的作用,其分子模型如图所示,下列关于白藜芦醇的说法错误的是( )
 现代科技证明,白藜芦主要来源于葡萄、花生、桑椹等植物,红葡萄酒中含有的白藜芦醇具有抗氧化、抗癌和预防心血管疾病的作用,其分子模型如图所示,下列关于白藜芦醇的说法错误的是( )
现代科技证明,白藜芦主要来源于葡萄、花生、桑椹等植物,红葡萄酒中含有的白藜芦醇具有抗氧化、抗癌和预防心血管疾病的作用,其分子模型如图所示,下列关于白藜芦醇的说法错误的是( )| A. | 白藜芦醇属于有机物,每个分子中含有29原子 | |
| B. | 白藜芦醇中氢元素的质量分数最小 | |
| C. | 白藜芦醇的分子式是C14H12O3 | |
| D. | 白藜芦醇中碳、氢、氧元素的个数比为3:12:14 |
17.下表所列各组物质中,只需通过一步反应就能实现图中箭头所示的转化的是( )
| 选项 | 物质转化关系 | a | b | c | d |
| A | 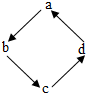 | Cu | CuO | CuSO4 | Cu(OH)2 |
| B | Na2CO3 | CaCO3 | CaO | Ca(OH)2 | |
| C | H2SO4 | Na2SO4 | BaSO4 | Ba(OH)2 | |
| D | CO2 | CaCO3 | H2O | O2 |
| A. | A | B. | B | C. | C | D. | D |
18.在化学王国里,数字被赋予了丰富的内涵.对下列化学用语中数字“2”的说法正确的是( )
①2H ②2NH3 ③SO2 ④$\stackrel{+2}{Cu}$O ⑤Mg2+.
①2H ②2NH3 ③SO2 ④$\stackrel{+2}{Cu}$O ⑤Mg2+.
| A. | 表示原子个数的是② | B. | 表示离子所带电荷数的是④ | ||
| C. | 表示分子中原子个数的是③ | D. | 表示分子个数的是① |