题目内容
向一定量的碳酸钙中加入100克溶质质量分数为7.3%的稀盐酸,恰好完全反应.请计算:(1)所用碳酸钙的质量;
(2)反应后所得溶液中溶质质量分数是多少?(结果保留到0.1%)
【答案】分析:写出化学方程式并代入反应的氯化氢的质量计算出碳酸钙、二氧化碳和氯化钙的质量,然后计算溶质的质量分数即可.
解答:解:设反应的碳酸钙质量是x 生成氯化钙的质量为y,二氧化碳的质量为z
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 111 44
x 100g×7.3% y z
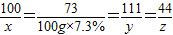
得:x=10g y=11.1g z=4.4g
∴反应后所得溶液的质量=10g+100g-4.4g=105.6g.
∴反应后溶液中溶质的质量分数=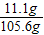 ×100%≈10.5%.
×100%≈10.5%.
答:(1)所用碳酸钙的质量是10g;(2)反应后溶液中溶质的质量分数为10.5%;
点评:掌握化学方程式的计算格式和规范性,注意:反应后溶液的质量等于反应前各物质的质量和减去气体的质量.
解答:解:设反应的碳酸钙质量是x 生成氯化钙的质量为y,二氧化碳的质量为z
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 111 44
x 100g×7.3% y z
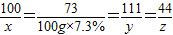
得:x=10g y=11.1g z=4.4g
∴反应后所得溶液的质量=10g+100g-4.4g=105.6g.
∴反应后溶液中溶质的质量分数=
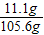 ×100%≈10.5%.
×100%≈10.5%.答:(1)所用碳酸钙的质量是10g;(2)反应后溶液中溶质的质量分数为10.5%;
点评:掌握化学方程式的计算格式和规范性,注意:反应后溶液的质量等于反应前各物质的质量和减去气体的质量.

练习册系列答案
 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目