题目内容
9. 溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据如图的溶解度曲线回答下列问题:
溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据如图的溶解度曲线回答下列问题:(1)20℃时,甲物质的溶解度小于 乙物质的溶解度(填“大于”、“等于”或“小于”).
(2)40℃时,两种物质的溶解度相等.
(3)60℃时,将40g 甲物质放入50g水中,所得溶液的质量为80g.
分析 根据固体物质的溶解度曲线可以比较不同物质在同一温度下的溶解度大小;60℃时,甲的溶解度为60g,100g水中只能溶解60g甲物质,故可求出所得溶液的溶质质量分数.
解答 解:由两物质的溶解度曲线可知,20℃时,甲物质的溶解度小于乙物质的溶解度.40℃时,两种物质的溶解度相等.60℃时,甲的溶解度为60g,50g水中只能溶解30g甲物质,
所得溶液的质量是30g+50g=80g.
故答案为:(1)小于;
(2)4;
(3)80g.
点评 本题难度不大,主要考查了根据固体物质的溶解度曲线解决相关的问题,培养学生的分析能力和解题能力.

练习册系列答案
相关题目
20.下列化学反应中,反应前后元素化合价均无变化的是( )
| A. | Na2O+H2O═2NaOH | B. | Na2SO4+4C═Na2S+4CO↑ | ||
| C. | Fe2O3+3CO═2Fe+3CO2 | D. | 2Al(OH)3═Al2O3+3H2O |
4.“酒香不怕巷子深”这句俗语说明( )
| A. | 在化学变化中,分子可分,而原子却不能再分 | |
| B. | 分子在不停地运动 | |
| C. | 分子由原子构成 | |
| D. | 分子的体积在变大 |
14.下列应用的原理(用化学方程式表示)及基本反应类型均正确的是( )
| A. | 用赤铁矿高炉炼铁 Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2置换反应 | |
| B. | 硫酸厂污水可用熟石灰中和处理 H2SO4+Ca(OH)2═CaSO4+H2O 复分解反应 | |
| C. | 加热混有二氧化锰的氯酸钾制取氧气 2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑分解反应 | |
| D. | 用红磷测定空气中氧气含量 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5氧化反应 |
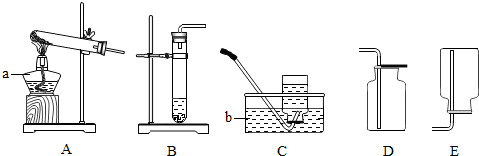
 如图所示是气体的发生装置和收集装置.
如图所示是气体的发生装置和收集装置. 查阅资料发现,氯化铵固体与亚硝酸钠固体混合加热也能制取氮气.反应的化学方程式如下:NH4Cl+NaNO2$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+2H2O+N2↑.
查阅资料发现,氯化铵固体与亚硝酸钠固体混合加热也能制取氮气.反应的化学方程式如下:NH4Cl+NaNO2$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+2H2O+N2↑.