题目内容
我校化学兴趣小组就空气中氧气的含量进行探究:如图1将红磷置于燃烧匙中燃烧,观察实验:

(1)为了充分消耗容器中的氧气,红磷的用量应 .
(2)红磷燃烧产生的现象: ,反应的文字表达式 ,红磷燃烧停止,等集气瓶冷却至室温时打开止水夹,可观察到水进入集气瓶约占总体积 ,该体积分数就是空气中氧气的含量.
【拓展】小莉同学对药品的选择产生了兴趣,提出问题:镁条能否代替红磷用于测定氧气的含量.于是设计如图2装置进行镁条在空气中燃烧的实验,燃烧冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
(3)燃烧冷却后打开止水夹,水能进入集气瓶的原因 .
(4)根据空气的组成,如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的 %.现进入集气瓶中水的体积约为其容积的70%,可推出减少的气体中肯定还有 .
【查阅资料】镁条在氮气中也能燃烧,产物为氮化镁(Mg3N2)固体.
(5)【结论】据此,镁条 (选填“能”或“不能”)用于测定氧气含量.写出镁条与氮气反应的文字表达式:
(6)【反思】同学们讨论后认为,该利用装置测定空气中氧气含量,药品的选择主要考虑以下因素中的 (填序号)
a.要能消耗氧气 b.不会跟空气中的其它成分反应
c.生成物不能为气体 d.药品用量是否充足.

(1)为了充分消耗容器中的氧气,红磷的用量应
(2)红磷燃烧产生的现象:
【拓展】小莉同学对药品的选择产生了兴趣,提出问题:镁条能否代替红磷用于测定氧气的含量.于是设计如图2装置进行镁条在空气中燃烧的实验,燃烧冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
(3)燃烧冷却后打开止水夹,水能进入集气瓶的原因
(4)根据空气的组成,如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的
【查阅资料】镁条在氮气中也能燃烧,产物为氮化镁(Mg3N2)固体.
(5)【结论】据此,镁条
(6)【反思】同学们讨论后认为,该利用装置测定空气中氧气含量,药品的选择主要考虑以下因素中的
a.要能消耗氧气 b.不会跟空气中的其它成分反应
c.生成物不能为气体 d.药品用量是否充足.
考点:测定空气里氧气含量的探究,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)红磷过量,可使集气瓶中的氧气完全消耗,减少误差;
(2)红磷剧烈燃烧、放出大量热和产生大量白烟,由于红磷消耗了空气中的氧气使集气瓶内的压强减小,打开止水夹后观察到:水沿导管倒流进入集气瓶中,倒流至集气瓶容积的
处;
(3)镁燃烧消耗集气瓶中的气体,导致集气瓶中的压强减小,冷却后打开止水夹时,在外界大气压的作用下,水会进入集气瓶.
(4)氧气在空气中的体积分数是21%,现进入集气瓶中水的体积约为其容积的70%,说明镁燃烧时,不仅消耗氧气,还消耗其它气体,因为消耗的气体很多,所以应该是至少消耗氮气;
(5)根据镁燃烧不仅消耗氧气,还消耗氮气等物质解答;
(6)根据测定氧气含量的实验原理分析.
(2)红磷剧烈燃烧、放出大量热和产生大量白烟,由于红磷消耗了空气中的氧气使集气瓶内的压强减小,打开止水夹后观察到:水沿导管倒流进入集气瓶中,倒流至集气瓶容积的
| 1 |
| 5 |
(3)镁燃烧消耗集气瓶中的气体,导致集气瓶中的压强减小,冷却后打开止水夹时,在外界大气压的作用下,水会进入集气瓶.
(4)氧气在空气中的体积分数是21%,现进入集气瓶中水的体积约为其容积的70%,说明镁燃烧时,不仅消耗氧气,还消耗其它气体,因为消耗的气体很多,所以应该是至少消耗氮气;
(5)根据镁燃烧不仅消耗氧气,还消耗氮气等物质解答;
(6)根据测定氧气含量的实验原理分析.
解答:解:
(1)红磷过量,可使集气瓶中的氧气完全消耗;
(2)步骤②集气瓶中的现象是:红磷剧烈燃烧、放出大量热和产生大量白烟;反应物是磷和氧气,生成物是五氧化二磷,反应条件是加热,所以文字表达式是:磷+氧气
五氧化二磷;由于红磷消耗了空气中的氧气使集气瓶内的压强减小,打开止水夹后观察到的现象是:水沿导管倒流进入集气瓶中,倒流至集气瓶容积的
处,可以得出空气中氧气的体积分数约为
;
(3)冷却后打开止水夹,水能进入集气瓶的原因是:集气瓶中的气体被消耗,压强减小,在外界大气压的作用下,水进入集气瓶.
故填:集气瓶中的气体被消耗,压强减小,在外界大气压的作用下,水进入集气瓶;
(4)点燃条件下,镁能和空气中的氧气、氮气、二氧化碳等物质反应,如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的21%,现进入集气瓶中水的体积约为其容积的70%,说明镁燃烧不仅消耗氧气,还消耗氮气等物质.
(5)镁燃烧不仅消耗氧气,还消耗氮气等物质,据此,镁条不能用于测定氧气含量.写出镁条与氮气反应的文字表达式为:镁+氮气
氮化镁;
(6)用燃烧法测定空气中氧气含量的实验时,利用的原理是物质燃烧只消耗氧气,生成物是固体,瓶内气体减小,水倒流,倒流入水的体积即为减少的氧气的体积,因此反应物应只与氧气反应,生成物应是固体才可以.
答案:
(1)充分反应掉集气瓶中的氧气
(2)红磷剧烈燃烧、放出大量热和产生大量白烟 磷+氧气
五氧化二磷
(3)集气瓶中的气体被消耗,压强减小,在外界大气压的作用下,水进入集气瓶
(4)21 氮气
(5)不能 镁+氮气
氮化镁
(6)abcd
(1)红磷过量,可使集气瓶中的氧气完全消耗;
(2)步骤②集气瓶中的现象是:红磷剧烈燃烧、放出大量热和产生大量白烟;反应物是磷和氧气,生成物是五氧化二磷,反应条件是加热,所以文字表达式是:磷+氧气
| 点燃 |
| 1 |
| 5 |
| 1 |
| 5 |
(3)冷却后打开止水夹,水能进入集气瓶的原因是:集气瓶中的气体被消耗,压强减小,在外界大气压的作用下,水进入集气瓶.
故填:集气瓶中的气体被消耗,压强减小,在外界大气压的作用下,水进入集气瓶;
(4)点燃条件下,镁能和空气中的氧气、氮气、二氧化碳等物质反应,如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的21%,现进入集气瓶中水的体积约为其容积的70%,说明镁燃烧不仅消耗氧气,还消耗氮气等物质.
(5)镁燃烧不仅消耗氧气,还消耗氮气等物质,据此,镁条不能用于测定氧气含量.写出镁条与氮气反应的文字表达式为:镁+氮气
| 点燃 |
(6)用燃烧法测定空气中氧气含量的实验时,利用的原理是物质燃烧只消耗氧气,生成物是固体,瓶内气体减小,水倒流,倒流入水的体积即为减少的氧气的体积,因此反应物应只与氧气反应,生成物应是固体才可以.
答案:
(1)充分反应掉集气瓶中的氧气
(2)红磷剧烈燃烧、放出大量热和产生大量白烟 磷+氧气
| 点燃 |
| 1 |
| 5 |
(3)集气瓶中的气体被消耗,压强减小,在外界大气压的作用下,水进入集气瓶
(4)21 氮气
(5)不能 镁+氮气
| 点燃 |
(6)abcd
点评:本题考查学生对实验原理与实验操作的理解与评价等,难度中等,清楚实验原理是解题的关键,需要学生具备扎实的基础知识与综合运用知识分析问题、解决问题的能力.

练习册系列答案
相关题目
以下有关水的说法中不正确的是( )
| A、实验室中常用水作溶剂配制溶液 |
| B、电解水实验证明水是由氢、氧两种元素组成的 |
| C、水(H2O)和过氧化氢(H2O2)分子中都含有氢气分子 |
| D、常用吸附,沉淀、过滤和蒸馏等方法净化水 |
如图实验操作错误的是( )
A、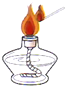 点燃酒精灯 |
B、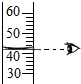 读出水的体积 |
C、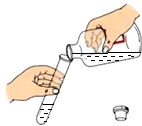 倾倒液体 |
D、 检查气密性 |
据中国之声《新闻纵横》2014年5月11日报道,在南京某工程队因探伤作业时操作不当丢失放射源铱(Ir)-192.符号“Ir”不能表示( )
| A、铱元素 | B、金属铱 |
| C、一个铱原子 | D、一个铱分子 |
在一密闭容器内有X、Y、Z、M四种物质,加热一段时间后停止反应,测得反应前后各物质的质量如表所示,则下列说法中不正确的是( )
| 物 质 | X | Y | Z | W |
| 反应前质量/g | 60 | 5 | 10 | 2 |
| 反应后质量/g | a | 5 | 32 | 20 |
| A、a等于20 |
| B、Y一定是催化剂 |
| C、继续加热至完全反应,还会有9g物质W生成 |
| D、反应消耗或生成的X、Z、W质量比为20:11:9 |
 某化学课外小组的同学,在实验室实验时发现一瓶标签破损的无色溶液(如图).这瓶溶液是什么物质?在老师的指导下,同学们首先提出假设并进行了如下的探究活动.请在空白处完成相应的内容.
某化学课外小组的同学,在实验室实验时发现一瓶标签破损的无色溶液(如图).这瓶溶液是什么物质?在老师的指导下,同学们首先提出假设并进行了如下的探究活动.请在空白处完成相应的内容.