题目内容
发射“嫦娥一号”的火箭用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作常规推进剂,其完全反应的化学方程式:C2H8N2+2N2O4
3N2+2CO2+4H2O,若燃烧3t偏二甲肼,试求消耗四氧化二氮的质量是多少?
| ||
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据反应的化学方程式可判断反应中偏二甲肼与四氧化二氮的质量关系,利用该质量关系可由燃烧偏二甲肼的质量计算出所消耗的四氧化二氮的质量.
解答:解:设消耗四氧化二氮的质量为x
C2H8N2+2N2O4
2CO2↑+4H2O+3N2↑,
60 184
3t x
=
x=9.2t
答:消耗四氧化二氮的质量是9.2t
C2H8N2+2N2O4
| ||
60 184
3t x
| 60 |
| 3t |
| 184 |
| x |
x=9.2t
答:消耗四氧化二氮的质量是9.2t
点评:根据反应的化学方程式可表示反应中各物质的质量比,可利用化学方程式由反应中一种物质的质量计算反应中其它物质的质量.

练习册系列答案
相关题目
 如果将物质按单质、氢氧化物、酸、碱、盐、有机物分类,图中甲、乙、丙是三种不同类别的物质,且相连物质之间均能发生化学反应,下列说法不符合图示要求的是( )
如果将物质按单质、氢氧化物、酸、碱、盐、有机物分类,图中甲、乙、丙是三种不同类别的物质,且相连物质之间均能发生化学反应,下列说法不符合图示要求的是( )| A、当甲为硝酸铵时,X可以为氢氧化钙 |
| B、当甲、乙、丙分别为酸、碱、盐时,X可能为碳酸钠 |
| C、当X为氧气时,甲、乙、丙可以为氢气、红磷、葡萄糖 |
| D、当X为稀盐酸时,甲、乙、丙可以为氧化铜、氢氧化铜、硝酸银 |
下列变化中,属于化学变化的是( )
| A、干冰升华 | B、灯管发亮 |
| C、铁丝弯曲 | D、酒精燃烧 |
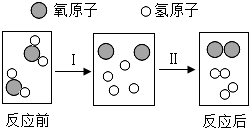 生产、生活、科技、环保等都离不开化学.
生产、生活、科技、环保等都离不开化学. ”表示一个氮分子,则“
”表示一个氮分子,则“ ”表示
”表示

 第22届冬季奥林匹克运动会,于2014年2月7日至23日在俄罗斯联邦索契市举行,乙基雌烯醇是一种参赛运动员禁用的兴奋剂,其化学式为C20H32O.乙基雌烯醇由
第22届冬季奥林匹克运动会,于2014年2月7日至23日在俄罗斯联邦索契市举行,乙基雌烯醇是一种参赛运动员禁用的兴奋剂,其化学式为C20H32O.乙基雌烯醇由