题目内容
16.某化学研究性小组进行了氨气的制取和有关性质的探究实验.
资料卡片:氨气通常情况下是无色、有刺激性气味的气体,密度比空气小,能使湿润的红色石蕊试纸变蓝,极易溶于水.浓氨水具有挥发性,加热熟石灰和氯化铵固体混合物可以生成氨气,若要快速产生氨气,可以将浓氨水滴加到生石灰中 请根据有关信息回答下列问题:
(1)写出利用装置A制取氨气的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
(2)将浓氨水滴加到生石灰中可以快速产生氨气,发生装置最好选用B(选字母).用此装置还可制取另一种气体,写出反应的化学方程式Zn+H2SO4=ZnSO4+H2↑或者2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑或者CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)研究性学习小组用D装置收集氨气,多余的气体用E装置吸收.写出所选用装置的导管口从左到右的正确连接顺序A→bac(用a、b、c表示).
(4 )闻氨气的气味时的注意事项是什么?
(5)若将制取氨气的熟石灰溶于水,形成的饱和溶液置于小烧杯许放入一只大 烧杯(如图2),在大烧杯中先加入一定量的水,再加入下列物质,观察到小烧杯中饱和溶液变浑浊,则加入的物质是AD(填字母).
A.浓琉酸 B.氯化钠固体C.硝酸铵固体D.氢氧化钠固体
(6)实验室常用74g熟石灰与氯化铵反应制取氨气,并将制得的气体通入一定量的稀硫酸中,可以制得一种化肥--硫酸铵.其反应的化学方程式为2NH3+H2SO4=(NH4)2SO4.计算理论上最多可制得硫酸铵的质量.
分析 (1)根据给出的氨气制取的方法写出化学方程式;
(2)将浓氨水滴加到生石灰中可以快速产生氨气,根据固液常温反应制取气体选择.固液常温反应还可以是实验室用锌和稀硫酸制取氢气或者是过氧化氢溶液在二氧化锰的催化下制取氧气或者碳酸钙和盐酸反应制取二氧化碳.
(3)氨气有毒,所以要进行尾气处理;
(4 )由于氨气有毒,所以闻氨气的气味时要轻轻在瓶口用手扇动使少许气体进入鼻孔即可;
(5)熟石灰溶解度随温度升高而减小,如果是饱和溶液变浑浊,则加入的物质应该能够溶解或者反应放热;
(6)根据熟石灰的质量和关系式法求算硫酸铵的质量,而不要先求氨气再求硫酸铵.
解答 解:(1)加热熟石灰和氯化铵固体混合物可以生成氨气,是固体加热制取氨气,所以用装置A制取氨气,是熟石灰和氯化铵在加热的条件下生成氯化钙和氨气以及水,对应的化学方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
(2)将浓氨水滴加到生石灰中可以快速产生氨气,是固液常温下制取气体,发生装置最好选用 B(选字母).用此装置还可制取氢气或者氧气或者二氧化碳等,写出反应的化学方程式 Zn+H2SO4=ZnSO4+H2↑或者2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑或者CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)研究性学习小组用D装置收集氨气,多余的气体用E装置吸收.由于氨气密度小,且极易溶解于水,所以连接顺序A→bac.
(4 )由于氨气有毒,所以要避免接触过多的氨气,所以闻氨气的气味时要轻轻在瓶口用手扇动使少许气体进入鼻孔即可;
(5)若将制取氨气的熟石灰溶于水,形成的饱和溶液置于小烧杯许放入一只大 烧杯(如图2),在大烧杯中先加入一定量的水,观察到小烧杯中饱和溶液变浑浊.由于熟石灰溶解度随温度升高而减小,则观察到小烧杯中饱和溶液变浑浊说明加入的物质溶解或者反应放热.
A.浓琉酸溶解于水放热,正确;
B.氯化钠固体溶解于水温度无明显变化,错误;
C.硝酸铵固体溶解于水温度降低,错误;
D.氢氧化钠固体溶解于水放热,正确;
故选:AD.
(6)设生成的硫酸铵的质量为x
由Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O和2NH3+H2SO4=(NH4)2SO4.可得关系式为.
Ca(OH)2∽∽∽2NH3∽∽∽(NH4)2SO4.
74 132
74g x
$\frac{74}{132}$=$\frac{74g}{x}$
x=132g
故答案为:
(1)Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
(2)B; Zn+H2SO4=ZnSO4+H2↑或者2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑或者CaCO3+2HCl═CaCl2+H2O+CO2.
(3)bac;
(4 )要轻轻在瓶口用手扇动使少许气体进入鼻孔即可;
(5)AD(填字母).
(6)132g.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案| A. | 用明矾溶液可以区分硬水和软水 | |
| B. | 净水操作中,相对净水程度最高的是蒸馏 | |
| C. | 加活性炭吸附的净水方式可以降低水的硬度 | |
| D. | 通过过滤的方法可以将水中所有杂质与水分离开来 |
| A. |  检査装置气密性 | B. |  蒸发食盐水 | C. |  移走蒸发皿 | D. |  过滤 |
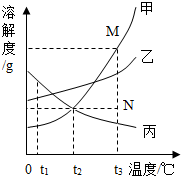 如图是甲、乙、丙三种物质的溶解度曲线.下列叙述正确的是( )
如图是甲、乙、丙三种物质的溶解度曲线.下列叙述正确的是( )| A. | t2℃时,甲、丙两种溶液中溶质的质量分数相等 | |
| B. | 将甲、乙的饱和溶液分别从t1℃升温到t2℃,溶质质量分数都变大 | |
| C. | t3℃时,组成为N点的甲溶液可通过增加溶质变为M点的溶液 | |
| D. | 将t3℃时的甲、乙饱和溶液降温到t2℃,甲析出晶体的质量一定大于乙 |
| A. | 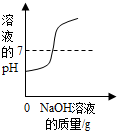 向一定量的稀H2SO4中滴入NaOH溶液 | |
| B. | 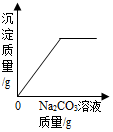 向一定量的稀HC1和CaCl2混合溶液中滴入Na2CO3溶液 | |
| C. | 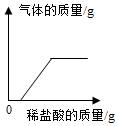 向一定量久置在空气中的NaOH溶液中滴加稀盐酸 | |
| D. | 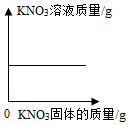 向一定量KNO3的饱和溶液中加人KNO3固体 |
| A. | 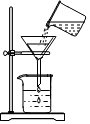 过滤 | B. | 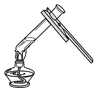 加热液体 | ||
| C. | 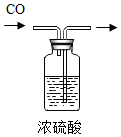 除去CO中的水蒸气 | D. | 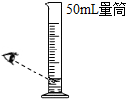 量取9.3mL液体 |
| A. | CO2、SO2、CO都是非金属氧化物,它们都能被氢氧化钠溶液吸收 | |
| B. | 氢氧化钠、氢氧化钙、氢氧化铜都是碱,它们都能使酚酞试液变红色 | |
| C. | H2、CO和CH4三种气体可作燃料,是因为都能燃烧并发出大量的热 | |
| D. | 用湿润的pH试纸测定某稀酸溶液的pH,测得的pH会偏小 |
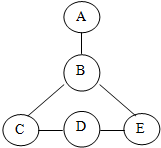 已知A~E是初中化学中常见的物质,它们之间的关系如图所示,相互之间的连线表示能发生化学反应.已知D是一种碱;C与E物质类别不同,且C是汽车用铅蓄电池的填充物质;B与E发生置换反应;A与B反应时火星四射.C的化学式是H2SO4; A物质具有的用途是供给呼吸(写一种即可);写出D与E反应的化学方程式2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.
已知A~E是初中化学中常见的物质,它们之间的关系如图所示,相互之间的连线表示能发生化学反应.已知D是一种碱;C与E物质类别不同,且C是汽车用铅蓄电池的填充物质;B与E发生置换反应;A与B反应时火星四射.C的化学式是H2SO4; A物质具有的用途是供给呼吸(写一种即可);写出D与E反应的化学方程式2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.