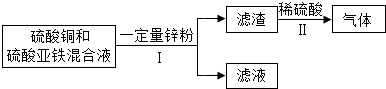
题目内容
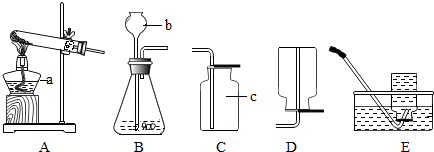
(1)根据如图1所示,回答有关问题:
①实验室用高锰酸钾制取氧气,应选用的发生装置是 (填字母),实验时该装置试管口应放一团棉花,其目的是 ;写出用氯酸钾和二氧化锰制取氧气的方程式 .
②实验室用锌粒与稀硫酸制取氢气,氢气密度比空气小,难溶于水,反应的化学方程式为 ,发生装置若用C装置代替B装置其优点是 ,如果用E装置收集该气体,则气体应从 端进入(填“b”或“c”).
(2)汽车、电动车一般使用铅酸蓄电池.某铅酸蓄电池使用的酸溶液是质量分数为20%的稀硫酸.请回答下列有关问题:
①若用100g质量分数为98%的浓硫酸(密度为1.84g/cm3)配制该稀硫酸时,需要蒸馏水(密度为1g/cm3)的体积为 mL(精确到0.1);
②该实验的主要步骤有计算、量取、稀释配制、装瓶并贴标签,请填写如图2所示的标签;
③用量筒量取浓硫酸时俯视读数,所配溶液溶质质量分数 20%(填“大于”、“小于”或“等于”).
①实验室用高锰酸钾制取氧气,应选用的发生装置是
②实验室用锌粒与稀硫酸制取氢气,氢气密度比空气小,难溶于水,反应的化学方程式为

(2)汽车、电动车一般使用铅酸蓄电池.某铅酸蓄电池使用的酸溶液是质量分数为20%的稀硫酸.请回答下列有关问题:
①若用100g质量分数为98%的浓硫酸(密度为1.84g/cm3)配制该稀硫酸时,需要蒸馏水(密度为1g/cm3)的体积为
②该实验的主要步骤有计算、量取、稀释配制、装瓶并贴标签,请填写如图2所示的标签;
③用量筒量取浓硫酸时俯视读数,所配溶液溶质质量分数
考点:常用气体的发生装置和收集装置与选取方法,一定溶质质量分数的溶液的配制,实验室制取氧气的反应原理,氢气的制取和检验,书写化学方程式、文字表达式、电离方程式
专题:溶液、浊液与溶解度,常见气体的实验室制法、检验、干燥与净化
分析:制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热,加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集;发生装置若用C装置代替B装置其优点是:可以控制反应的发生和停止;如果用E装置收集该气体,则气体应从短管进入,因为氢气的密度比空气的密度小;设需要蒸馏水的质量为x,100g×98%=(100g+x)×20%,x=390g;v=
=
=390.0mL;标签的内容是:名称稀硫酸,质量分数20%;用量筒量取浓硫酸时俯视读数,实际浓硫酸量少了,因此所配溶液溶质质量分数小于20%.
| m |
| ρ |
| 390g |
| 1.0g/mL |
解答:解:(1)如果用高锰酸钾制氧气就需要加热,加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集;发生装置若用C装置代替B装置其优点是:可以控制反应的发生和停止;如果用E装置收集该气体,则气体应从短管进入,因为氢气的密度比空气的密度小;故答案为:①A;为了防止高锰酸钾粉末进入导管;2KClO3
2KCl+3O2↑;②Zn+H2SO4=ZnSO4+H2↑;可以控制反应的发生和停止;c;
(2)设需要蒸馏水的质量为x,100g×98%=(100g+x)×20%,x=390g;v=
=
=390.0mL;标签的内容是:名称稀硫酸,质量分数20%;用量筒量取浓硫酸时俯视读数,实际浓硫酸量少了,因此所配溶液溶质质量分数小于20%;故答案为:①390.0mL;②稀硫酸;20%;③小于;
| ||
| △ |
(2)设需要蒸馏水的质量为x,100g×98%=(100g+x)×20%,x=390g;v=
| m |
| ρ |
| 390g |
| 1.0g/mL |
点评:本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、溶液的稀释问题和有关的计算等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
家庭常用液体的pH如下,其中碱性最强的是( )
| A、洁厕精:1.0 |
| B、洗发露:7.6 |
| C、洗衣液:10.5 |
| D、漂白液:13.4 |
纳米二氧化钛(TiO2)可净化室内空气,TiO2中Ti的化合价为( )
| A、+4 | B、+2 | C、-2 | D、-4 |
有关H2,C、CO三种物质的下列说法正确的是( )
| A、都是目前最理想的清洁燃料 |
| B、与CuO反应后,一定有化合物生成 |
| C、与CuO发生的反应都属于置换反应 |
| D、与等质量的CuO反应,所需H2,C,CO三种物质的质量之比1:6:14 |
下列实验操作中,正确的是( )
A、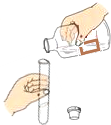 倾倒液体 |
B、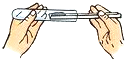 取用固体粉末 |
C、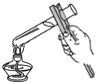 加热液体 |
D、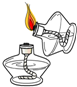 点燃酒精灯 |