题目内容
14.如图所示为实验室常见气体制备,净化、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器).某学校两个化学实验探究小组的同学欲用他们完成各自的探究实验.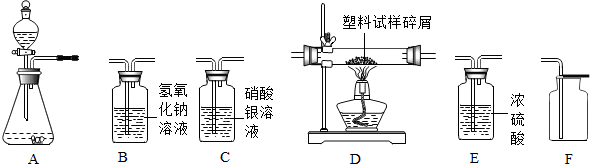
(1)第一组的同学以石灰石和稀盐酸为原料,在实验室中制备、收集干燥纯净的二氧化碳气体,按照要连接仪器,并检验装置的气密性.
①所选仪器的连接顺序为A→C→E→F(填写仪器序号字母).
②仪器A中,发生反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O.
③若将二氧化碳气体通入氢氧化钠溶液中,至恰好完全反应,所得溶液显碱性填“酸性”“碱性”“中性”之一).
(2)第二组的同学以过氧化氢溶液为原料(MnO2为催化剂)制备氧气,并对某种塑料的组成元素进行分析探究(资料显示该塑料只含C,H,O三种元素),所选仪器按“A→E1→D→E2→B→碱石灰干燥管”的顺序连接,(B1,B2为浓硫酸洗气瓶),实验前检验装置气密性.使该塑料试样碎屑在纯氧气中充分燃烧,观察现象,收集有关实验数据(假设发生的化学反应都充分反应),试回答下列问题:
①仪器A中所发生反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
②上述连接中装置B的作用是吸收反应生成的二氧化碳.
③仪器D的玻璃管中放入的塑料试样碎屑质量为Wg,塑料试样充分燃烧后,测得仪器E2质量增加a g,仪器B质量增加b g,则Wg该塑料试样中含氧元素的质量为(W-$\frac{a}{9}$-$\frac{3b}{11}$)g (计算结果可为分数形式).
④若装置中没有连接仪器E1,这样测算出的该塑料试样中氢元素的质量与实际值比较将偏大 (填“偏小”“偏大”“基本一致”之一).
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;硝酸银溶液除去氯化氢气体,二氧化碳可以用浓硫酸干燥.若将二氧化碳气体通入氢氧化钠溶液中,至恰好完全反应,所得溶液显碱性,因为二氧化碳与氢氧化钠反应生成碳酸钠和水,碳酸钠溶液显碱性;有关的计算要准确,结果后要有单位.
解答 解:(1)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;硝酸银溶液除去氯化氢气体,二氧化碳可以用浓硫酸干燥;若将二氧化碳气体通入氢氧化钠溶液中,至恰好完全反应,所得溶液显碱性,因为二氧化碳与氢氧化钠反应生成碳酸钠和水,碳酸钠溶液显碱性;故答案为:①A→C→E→F ②CaCO3+2HCl=CaCl2+CO2↑+H2O ③碱性
(2)如果用双氧水和二氧化锰制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;氧元素的质量等于塑料的质量减去碳元素的质量,再减去氢元素的质量;若没有E1,则A中水蒸气进入E2使a偏大,氢元素质量为$\frac{a}{9}$,故偏大.故答案为:①2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑②吸收反应生成的二氧化碳 ③(W-$\frac{a}{9}$-$\frac{3b}{11}$)g;④偏大
点评 本考点主要考查了气体的干燥和除杂、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和有关的计算等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 小学课时特训系列答案
小学课时特训系列答案| A. | 桌面上酒精灯内酒精洒出,着火燃烧,立即用湿抹布扑灭 | |
| B. | 厨房内管道煤气(主要成分是CO)泄漏,立即关闭阀门并开窗通风 | |
| C. | 进入深洞,燃着的火把熄灭立即停止前进,退出山洞 | |
| D. | 炒菜时油锅着火,立刻浇水灭火 |
| A. | 硫粉 | B. | 铁丝 | C. | 木炭 | D. | 红磷 |
| A. | 给试管里的液体加热时,试管口对着没有人的方向 | |
| B. | 洒出的少量酒精在桌面上燃烧起来,立即用湿抹布盖灭 | |
| C. | 向试管内加液体时,将胶头滴管伸入试管内进行滴加 | |
| D. | 做铁丝在氧气中燃烧实验时,预先在集气瓶底铺一层细沙 |
| A. | NaOH、CuSO4、H2SO4 | B. | NaCl、Ba(NO3)2、HCl | ||
| C. | NaCl、Na2SO4、Na2CO3 | D. | NH4NO3、NaOH、NaCl |
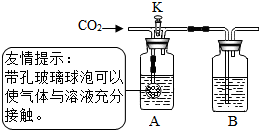
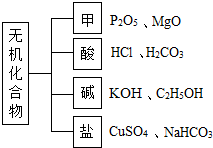 如图是小宇同学对常见化合物的分类整理.
如图是小宇同学对常见化合物的分类整理.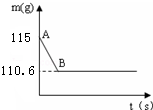 鸡蛋壳的主要成分是碳酸钙,某兴趣小组为了测定鸡蛋壳中CaCO3的含量,现取15g鸡蛋壳捣碎,放在烧杯中,然后向其中加入100g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用盐酸刚好消耗了加入量的一半.试计算:
鸡蛋壳的主要成分是碳酸钙,某兴趣小组为了测定鸡蛋壳中CaCO3的含量,现取15g鸡蛋壳捣碎,放在烧杯中,然后向其中加入100g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用盐酸刚好消耗了加入量的一半.试计算: