��Ŀ����
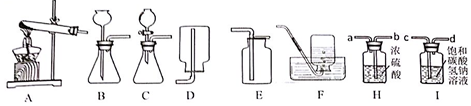
16�������仯����������������Ҫ�����ã���ش��������⣺��1������ϸ��˿��������ȼ�յ�ʵ��ʱ��Ϊ�˷�ֹ����ƿը�ѣ�����ȡ�Ĵ�ʩ���ڼ���ƿ�ײ���������ˮ��ϸɳ��
��2�������������������Ʋ�����Һ����CuSO4�������û�ѧ����ʽ��ʾ��ԭ��Fe+CuSO4=FeSO4+Cu��
��3������Ʒ�ڳ�ʪ�Ŀ����������⣬�������Ҫ�ɷ���Fe2O3���ѧʽ����
��4�������ۺ�ͭ�۵Ļ���������������Һ�У���Ӧ�������й���ʣ�࣮����˵����ȷ����A����д��ĸ��ţ���
A��ʣ�����϶�������
B����Ӧ����Һ��һ����Ag+��Cu2+
C���������϶�������ͭ
D����Ӧ����Һ��һ����Fe2+��Cu2+��
���� ��1���������������ڵ�ȼ������������������������Ϊ�˷�ֹ����ƿը�ѣ��ڼ���ƿ�ײ���������ˮ��ϸɳ���з�����
��2��������������ͭ��Ӧ��������������ͭ���з�����
��3�������������Ҫ�ɷ������������з�����
��4�����ݽ������˳���֪������ǰ��Ľ������Խ����ں���Ľ�����������Һ���û��������з�����
��� �⣺��1�����������ڵ�ȼ������������������������Ϊ�˷�ֹ����ƿը�ѣ��ڼ���ƿ�ײ���������ˮ��ϸɳ��
��2����������ͭ��Ӧ��������������ͭ����ѧ����ʽΪ��Fe+CuSO4=FeSO4+Cu��
��3���������Ҫ�ɷ�������������ѧʽΪ��Fe2O3��
��4������ͭ�Ļ�Զ�����ǿ�����ܺ���������Һ��Ӧ�������Ļ�Դ���ͭ����Ӧ˳��Ϊ�������û�����������Ӧ��ͭ�ٷ�Ӧ��
A�����ڲ�֪������ͭ���������Բ����жϳ�ʣ�����ɷ��Ƿ�������ͭ��������ʣ�������һ������������A��ȷ��
B����������Ӧ����������������Һ��һ�������������ӣ����ڲ�֪���ӵ�����ͭ����������δ��Ӧ�꣬����Һ����Cu 2+����B����
C����A������֪�������п϶�����������ȷ���Ƿ�������ͭ����C����
D����Ӧ�����һ����������������δ��ȫ��Ӧ������Һ����Fe 2+��Ag+��Cu 2+������������ȫ��Ӧ������Һ����Ag+����D����
��ѡ��A��
�ʴ�Ϊ����1���ڼ���ƿ�ײ���������ˮ��ϸɳ��
��2��Fe+CuSO4=FeSO4+Cu��
��3��Fe2O3��
��4��A��
���� ���⿼���˽����Ļ�ѧ���ʺͽ������˳���Ӧ�ã�Ҫ�����ѧ֪ʶϸ�ķ������

 �ƸԴ��ž�ϵ�д�
�ƸԴ��ž�ϵ�д�| A�� | ����� | B�� | �Ȼ��� | C�� | ���� | D�� | ��� |
| A�� | ���ˮ������������������������2��1 | |
| B�� | ������������Ӧ����ˮ��˵��ˮ�����⡢������Ԫ����ɵ� | |
| C�� | ����ˮ�����ó��������ˡ�����������ķ�������ˮ | |
| D�� | ˮ�������к�������Ԫ�أ�ռ����������70%���� |
| A�� | BaCl2 H2SO4 HCl | B�� | NaOH KOH HCl | ||
| C�� | K2CO3 Na2CO3 KCl | D�� | NaCl NaOH HCl |