题目内容
20.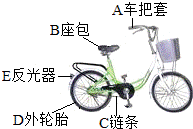 如图是同学们经常使用交通工具--自行车,请完成下列各题:
如图是同学们经常使用交通工具--自行车,请完成下列各题:(1)所标各部件中属于有机合成材料的是ABDE(填物质填序号).
(2)车轮的钢圈在潮湿的空气中会锈蚀,这是铁与空气中的氧气和水蒸气等物质发生化学反应的结果.通常用盐酸除铁锈,该反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O;
(3)新型食品保鲜剂“纳米α铁粉”被称为“双吸剂”,其实质就是利用了铁生锈的原理,若用化学方法检验使用一段时间的“纳米α铁粉”是否完全失效,可在样品中加入稀盐酸,若出现有气泡产生的现象,说明该双吸剂仍可使用.
分析 根据物质的类别、金属锈蚀的条件、氧化铁与盐酸反应化学方程式的书写以及铁与盐酸反应的现象进行分析解答即可.
解答 解:(1)据图可以看出,车把套是橡胶制成的、座包是橡胶制成的、外轮胎是橡胶制成的、反光器是塑料制成的,使用合成材料制成的,故填:ABDE;
(2)铁在与水和氧气并存时易生锈,氧化铁能与盐酸反应生成氯化铁和水,故填:氧气,Fe2O3+6HCl=2FeCl3+3H2O;
(3)若双吸剂可以使用,则含有铁,铁能与盐酸反应产生氢气,有气泡产生,故填:有气泡产生.
点评 本题考查的是金属材料的应用的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
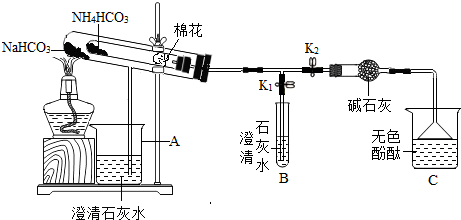
10.碳酸氢钠和碳酸氢铵(NH4HCO3)是制作油条和油饼时常用的膨松剂,某学校化学兴趣小组对这两种膨松剂受热分解后的产物进行了探究:
【查阅资料】
①碱石灰是固体氢氧化钠和氧化钙的混合物,不与氨气反应.
②氨气有刺激性气味,极易溶于水水溶液呈碱性.
【进行实验】
按如图所示连接好装置(夹持仪器略去).
【拓展反思】为了进一步确定NaHCO3受热分解后生成Na2CO3,后续的实验操作是加热至完全反应后,冷却,向大试管中加入适量的稀盐酸,把产生的气体通入澄清石灰水中.

【查阅资料】
①碱石灰是固体氢氧化钠和氧化钙的混合物,不与氨气反应.
②氨气有刺激性气味,极易溶于水水溶液呈碱性.
【进行实验】
按如图所示连接好装置(夹持仪器略去).
| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 连接好装置,关闭K1,打开K2微热左侧双层试管 | AC中均出现气泡 | 装置的气密性良好 |
| 打开K1,关闭K2,停止加热 | A、B烧杯中的导管内均形成一段稳定的液柱 | ||
| ② | 在试管中加入两种膨松剂,打开K1,关闭K2,点燃酒精灯加热双层试管 | 内层试管中白色固体明显减少,AB中澄清石灰水都变浑浊 | 均有二氧化碳生成 |
| ③ | 关闭K1,打开K2(开关操作) | 无色酚酞试液变红 | 碳酸氢铵分解生成了氨气 |
| ④ | 继续加热一段时间 | 外层试管中仍有固体 | NH4HCO3受热分解的化学方程式为NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑ |
11.下列变化属于化学变化的是( )
| A. | 湿衣服变干 | B. | 木棒折断 | C. | 燃放烟花 | D. | 蔗糖溶解 |
8.下列说法正确的是( )
| A. | 空气中氮气的体积分数为21% | |
| B. | 人体中含量最多的金属元素是钙元素 | |
| C. | 海洋中含量最多的非金属元素是氢元素 | |
| D. | 地壳中含量最多的金属元素是硅元素 |
15.2015年10月8日,屠呦呦教授获得诺贝尔生物学或医学奖,成为首获科学类诺贝尔奖的中国人,她因为发现了治疗疟疾的药物“青蒿素”,挽救了数百万人的生命.“青蒿素”的化学式为C15H22O5,下列关于“青蒿素”的说法错误的是( )
| A. | 青蒿素属于有机化合物 | |
| B. | 青蒿素中碳元素的质量分数为35.7% | |
| C. | 青蒿素由碳、氢、氧3种元素组成 | |
| D. | 青蒿素分子中碳、氢、氧的原子个数比为15:22:5 |
5.下列实验方法一定能达到实验目的是( )
| 选项 | 实验目的 | 试验方法 |
| A | 检验一瓶气体是否为CO2 | 将燃着的木条伸入瓶中 |
| B | 鉴别H2和CH4 | 分别点燃,在火焰上放罩一干冷烧杯 |
| C | 鉴别石灰水和NaOH溶液 | 加入适量的稀盐酸 |
| D | 除去CaO中的CaCO3 | 高温加热到固体质量不变 |
| A. | A | B. | B | C. | C | D. | D |
12.某兴趣小组用加热氯酸钾与二氧化锰混合物的方法制取氧气,试管中固体的质量随时间变化的数据见表,制取结束后,向剩余固体中加入85.1g水充分溶解后,过滤,回收二氧化锰固体,并得到氯化钾不饱和的溶液.
(1)共制得氧气9.6g.
(2)计算所得氯化钾溶液的溶质质量分数.
| 加热时间/min | 0 | t1 | t2 | t3 |
| 固体质量/g | 28.0 | 23.2 | 18.4 | 18.4 |
(2)计算所得氯化钾溶液的溶质质量分数.