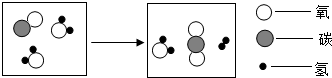
题目内容
20.甲、乙两图分别表示氯化钠和硝酸钾在水中的溶解度曲线.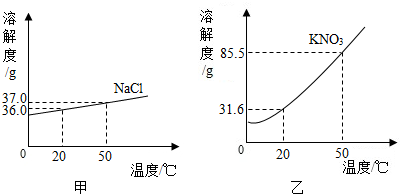
(1)比较甲、乙两图可知:影响固体物质溶解度曲线陡斜程度的因素是溶质的性质,两种物质中氯化钠的溶解度受温度影响更小.
(2)20℃时硝酸钾的溶解度为31.6g.
(3)若将20℃时硝酸钾的饱和溶液升温到50℃,此时溶液为不饱和溶液(填“饱和溶液”或“不饱和溶液”),溶液中硝酸钾的质量分数不变(填“变大”、“变小”或“不变”).
分析 (1)溶质的性质对溶解度影响很大;
(2)根据物质的溶解度曲线可以判断某一温度时物质溶解度的大小;
(3)饱和溶液和不饱和溶液之间可以相互转化;溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%.
解答 解:(1)影响固体物质溶解度曲线陡斜程度的因素是溶质的性质,两种物质中氯化钠的溶解度受温度影响更小.
故填:溶质的性质;氯化钠.
(2)由溶解度曲线可知,20℃时硝酸钾的溶解度为31.6g.
故填:31.6g.
(3)硝酸钾的溶解度随着温度的升高而增大,若将20℃时硝酸钾的饱和溶液升温到50℃,此时溶液为不饱和溶液;溶液中硝酸钾的质量不变,水的质量不变,因此溶质的质量分数不变.
故填:不饱和溶液;不变.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
15.为准确配制80g 10%的氯化钠溶液,要求尽量减小计量仪器称量时的误差.该实验用到了下列仪器,其中属于计量仪器的是( )
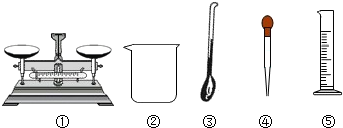

| A. | ①⑤ | B. | ③④⑤ | C. | ①③④⑤ | D. | ①②③④⑤ |
5.下图所示的实验操作中,正确的是( )
| A. | 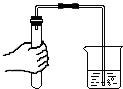 | B. | 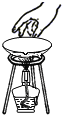 | C. |  | D. |  |
12.如图是四种粒子的结构示意图,对它们的描述正确的是( )
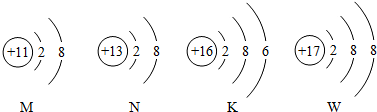
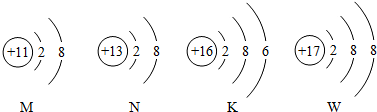
| A. | 四种粒子均表示原子 | |
| B. | N与W可形成NW3型化合物 | |
| C. | 四种粒子均达到了相对稳定结构 | |
| D. | 四种粒子所代表的元素不在同一周期 |

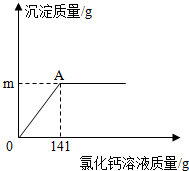 某纯碱样品中含有少量氯化钠,取该样品11g,全部溶液在100g水中,再逐渐滴加氯化钙溶液,反应的情况如图所示,A点时,过滤,得到滤液242g,计算:
某纯碱样品中含有少量氯化钠,取该样品11g,全部溶液在100g水中,再逐渐滴加氯化钙溶液,反应的情况如图所示,A点时,过滤,得到滤液242g,计算: