题目内容
20.硫酸亚铁是一种重要的食品和饲料添加剂,某补血剂样品 主要成分为硫酸亚铁晶体(FeSO4•xH2O),某化学兴趣小组对其产生了兴趣并进行了探究:【探究一】硫酸亚铁晶体(FeSO4•xH2O)热分解研究
【查阅资料】
1无水硫酸铜粉末遇水会变成蓝色的硫酸铜晶体;
2硫酸亚铁晶体加热时,先失去结晶水,高温会继续分解产生金属氧化物和气态非金属氧化物.
3二氧化硫能使高锰酸钾溶液褪色.
【进行实验】该兴趣小组同学称取27.8g硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行分析,并利用SDTQ600热分析仪,对硫酸亚铁晶体热分解获得相关数据,绘制成图2所示的关系图,试回答:

(1)装置B中硫酸铜粉末变蓝,说明产物中有水,该物质的质量是12.6gg;装置C中高锰酸钾溶液褪色,说明产物中还有SO2;硫酸亚铁晶体完全分解后,装置A中的固体呈红棕色,放入足量稀盐酸,固体全部溶解,且得到黄色溶液,则该红棕色固体与稀盐酸反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O.
(2)D装置中球形干燥管的作用是防止NaOH溶液倒吸.
(3)硫酸亚铁分解生成铁的氧化物和硫的两种氧化物,请写出化学反应方程式2FeSO4=Fe2O3+SO2↑+SO3↑.
(4)根据图2中的数据,请求出FeSO4•xH2O中的x=7.(不写过程)
【交流讨论】实验中要持续通入氮气,否则测出的x会偏小(填“偏大”、“偏小”或“不变”).
【探究二】补血剂样品中硫酸亚铁的含量:
①取10g补血剂样品研细后溶于40g水中,研细的目的是增大接触面积,使其充分溶解;
②向所配制的溶液中加氯化钡溶液至略过量,使其充分反应;
③过滤,洗涤,干燥,称量所得白色固体的质量为6.99g.
请计算出10g样品中FeSO4的质量分数,写出计算过程.
(已知:FeSO4+BaCl2=BaSO4↓+FeCl2,有关相对分子质量:FeSO4-152,BaSO4-233)
分析 探究一:为回收废水中的铜,可以使用活动性比铜活泼的金属比如铁将其置换出来;然后依据反应流程图分析所加入的金属和生成物,写出反应方程式;无水硫酸铜白色粉末遇水变蓝,故常用来检验水的存在,二氧化硫能使高锰酸钾溶液褪色;根据反应前后元素的种类不变及红棕色固体可与稀盐酸反应生成黄色溶液分析解答;硫酸亚铁分解生成的二氧化硫能造成空气污染,可以使用氢氧化钠溶液将其除去.
探究二:根据反应的化学方程式结合题干提供的数据进行解答.
解答 解:【探究一】
(1)无水硫酸铜白色粉末遇水变蓝,生成的水的质量为:27.8g-15.2g=12.6g;C中高锰酸钾溶液褪色,所以根据题意可知,硫酸亚铁晶体能分解生成二氧化硫;
氧化铁能与盐酸反应生成氯化铁和水,故答案为:水;12.6g;SO2;Fe2O3+6HCl=2FeCl3+3H2O.
(2)把球形干燥管插入氢氧化钠溶液中的作用是防止液体倒吸,反应生成的二氧化硫是空气污染气体,可以使用氢氧化钠溶液将其吸收;
故答案为:防止NaOH溶液倒吸.
(3)硫酸亚铁晶体分解生成氧化铁、二氧化硫和三氧化硫,故答案为:2FeSO4=Fe2O3+SO2↑+SO3↑;
(4)硫酸亚铁的质量为15.2g,水的质量为12.6g
FeSO4--xH2O
152 18x
15.2g 12.6g
$\frac{152}{18x}=\frac{15.2g}{126g}$
x=7
故答案为:7;
【交流讨论】实验中要持续通入氮气,否则是的质量偏小,测出的x会偏小,故答案为:偏小;
【探究二】
①取10g补血剂样品研细后溶于40g水中,研细的目的是增大接触面积,使其充分溶解,故填:增大接触面积,使其充分溶解;
②向所配制的溶液中加氯化钡溶液至略过量,使其充分反应;
③过滤,洗涤,干燥,称量所得白色固体的质量为6.99g.
请计算出10g样品中FeSO4的质量分数,写出计算过程.设硫酸亚铁的质量为x
FeSO4+BaCl2=BaSO4↓+FeCl2
152 233
x 6.99g
$\frac{152}{233}=\frac{x}{6.99g}$
x=4.56g
硫酸亚铁的质量分数为:$\frac{4.56g}{10g}×100%$=45.6%
故答案为:45.6%.
点评 本题是一道实验探究题,能较好的考查学生分析和解决问题的能力,考查了常见金属的性质以及某些盐的性质,解答时要依据题干提供信息,结合相关知识细心分析解答.

 全能练考卷系列答案
全能练考卷系列答案| A. | 酒精挥发 | B. | 厨房里的菜刀生锈 | ||
| C. | 冰受热熔化成水 | D. | 用木炭消除冰箱中的异味 |
| A. | 滤液N中可能有单质铁,也可能有单质镁 | |
| B. | 滤液M中至少含有两种金属阳离子 | |
| C. | 滤渣N的质量一定小于加入铁粉的质量 | |
| D. | 滤液M的颜色和原溶液的颜色一样 |
| A. | 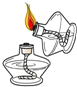 点燃酒精灯 | B. | 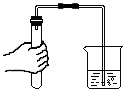 检查气密性 | C. | 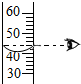 液体读数 | D. | 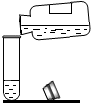 倾倒液体 |
| A. | 氯化钾溶液 | B. | 碳酸钠溶液 | C. | 氢氧化钠溶液 | D. | 硝酸银溶液 |
| A. | 食醋 | B. | 白酒 | C. | 铁锅 | D. | 水银 |
| A. | 只有② | B. | 只有②④ | C. | ①②④ | D. | 全部 |