题目内容
9.小华用氯酸钾和二氧化锰反应制取氧气,记录反应中固体质量随时间变化的数据如表:| 加热时间/min | 0 | t1 | t2 | t3 |
| 固体质量/g | 2.94 | 2.46 | 1.98 | 1.98 |
②计算参加反应的氯酸钾的物质的量.(根据化学方程式计算)
分析 氯酸钾受热分解生成氯化钾和氧气,反应前后的质量差即为反应生成氧气的质量,根据氧气质量可以计算反应的氯酸钾的质量.
物质的量n=$\frac{m}{M}$计算.
解答 解:①反应生成的气体质量为:2.94g-1.98g=0.96g,
故填:0.96.
②设参加反应的氯酸钾的物质的质量为x,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,
245 96
x 0.96g
$\frac{245}{x}$=$\frac{96}{0.96g}$,
x=2.45g,
n=$\frac{m}{M}$=$\frac{2.45g}{122.5g/mol}$=0.02mol.
答:参加反应的氯酸钾的物质的量是0.02mol.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

练习册系列答案
相关题目
19.分类方法是化学学习的重要方法,下列分类错误的是( )
| A. | 根据纯净物中元素的种类数,将其分为单质与化合物 | |
| B. | 根据一定温度下溶液能否再溶解溶质,将其分为饱和溶液与不饱和溶液 | |
| C. | 根据离子的电性,将其分为阳离子与阴离子 | |
| D. | 根据溶质的多少,将溶液分为浓溶液和稀溶液 |
20.下列变化中,属于化学变化的是( )
| A. | 干冰升华 | B. | 石蜡熔化 | C. | 酒精挥发 | D. | 粮食酿酒 |
17.关于物质在空气中燃烧的现象描述正确的是( )
| A. | 木炭:发出白光 | B. | 铁丝:火星四射 | C. | 红磷:大量白雾 | D. | 硫粉:淡蓝色火焰 |
4.现有一包CaCl2和Ca(ClO)2混合物,其中氯元素的质量百分含量为53.75%,则混合物中 氧元素的质量百分含量可能是( )
| A. | 44.5% | B. | 16% | C. | 20% | D. | 32% |
14.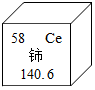 铈是一种稀土元素,在元素周期表中铈元素的某些信息如图所示,下列有关铈的说法正确的是( )
铈是一种稀土元素,在元素周期表中铈元素的某些信息如图所示,下列有关铈的说法正确的是( )
 铈是一种稀土元素,在元素周期表中铈元素的某些信息如图所示,下列有关铈的说法正确的是( )
铈是一种稀土元素,在元素周期表中铈元素的某些信息如图所示,下列有关铈的说法正确的是( )| A. | 元素符号为Ce | B. | 原子核内中子数为58 | ||
| C. | 相对原子质量140.1g | D. | 属于非金属元素 |
1.若将 100g 10%的稀盐酸 与 100g 10%的氢氧化钠溶液充分混合反应,下列说法错误的是( )
| A. | 该反应属于中和反应 | |
| B. | 该反应的化学方程式可用来表示治疗胃酸过多的反应原理 | |
| C. | 该反应所得的溶液中含有两种溶质 | |
| D. | 该反应的实质是 H+和 OH-结合生成 H2O |
18. 硝酸钾是常见的化学肥料.
硝酸钾是常见的化学肥料.
资料:硝酸钾的溶解度数据如表所示:
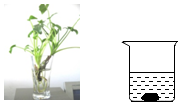
(1)小刚想要配制一份硝酸钾的饱和溶液,在烧杯中放入100g水,将称好的31.6g硝酸钾放入烧杯中,搅拌10分钟,却出现了如图中烧杯所示的现象.此时环境的温度可能是<20℃(填“>”、“<”或“=”).
(2)小刚要使未溶解的固体溶解,可以采取的措施是升温或加入适量水.
(3)查阅资料,小刚发现硝酸钾溶液可用作无土栽培的营养液,但浓度不能高于1%.小刚要帮妈妈配制硝酸钾溶液用于养花,若称取2g硝酸钾固体,加入水的体积最少为198ml(如不能整除结果保留一位小数,水的密度为1g/cm3).
 硝酸钾是常见的化学肥料.
硝酸钾是常见的化学肥料.资料:硝酸钾的溶解度数据如表所示:
| 温度/℃ | 10 | 20 | 30 | 40 | 50 |
| 溶解度/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 |
(2)小刚要使未溶解的固体溶解,可以采取的措施是升温或加入适量水.
(3)查阅资料,小刚发现硝酸钾溶液可用作无土栽培的营养液,但浓度不能高于1%.小刚要帮妈妈配制硝酸钾溶液用于养花,若称取2g硝酸钾固体,加入水的体积最少为198ml(如不能整除结果保留一位小数,水的密度为1g/cm3).
19.如图实验操作正确的是( )
| A. |  熄灭酒精灯 | B. |  闻气体气味 | ||
| C. |  称量NaCI固体 | D. |  取用液体 |